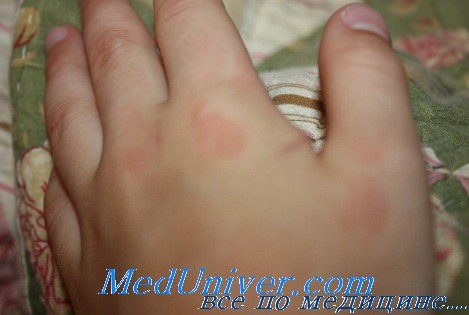
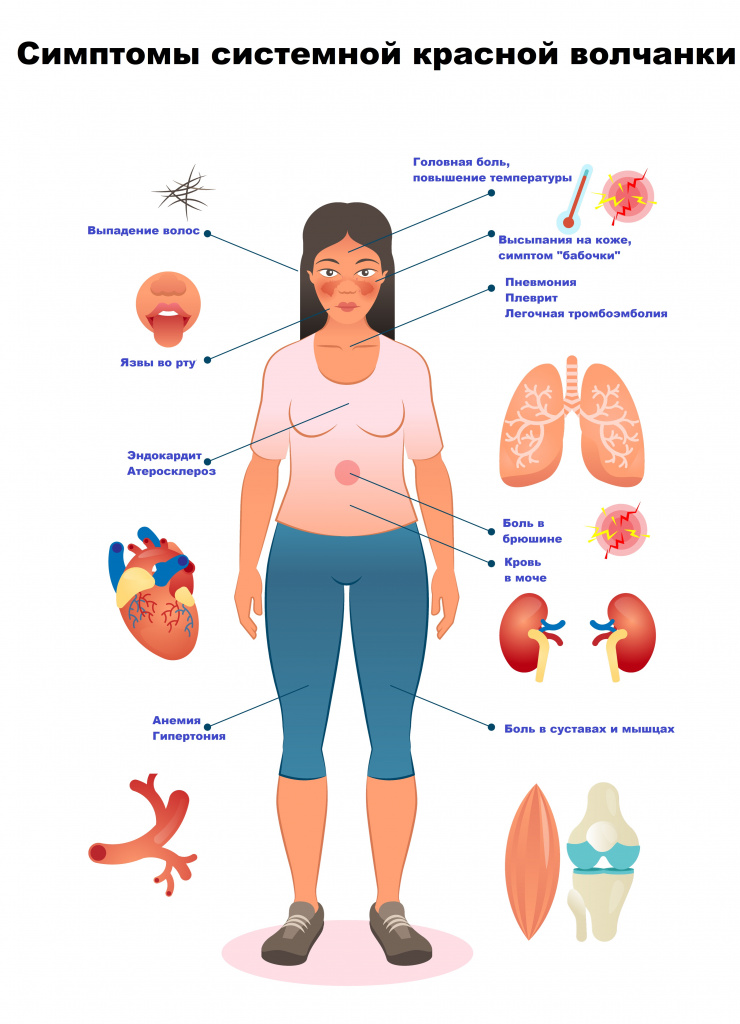
Патогенез ревматоидного артрита
Ревматоидный артрит является системной патологией. Страдают не только суставы, но и внутренние органы. Это обусловлено патогенезом ревматоидного артрита – поражается соединительная ткань, которая есть везде. До сих пор точно не установлены причины возникновения болезни у человека. Распространенность заболевания колеблется от 0,5 до 2% населения. Чаще страдают женщины. Является причиной инвалидности у людей трудоспособного возраста.
Этиология
До настоящего времени этиология ревматоидного артрита не установлена. Существует несколько теорий, объясняющих возникновение воспалительного процесса в суставах:
- Инфекционная. Провокаторами заболевания могут быть вирус Эпштейн-Барра, Т-клеточный вирус, парвовирус. Это подтверждается тем, что у 80% пациентов обнаруживались антитела к вирусу Эпштейн-Барра;
- Генетическая предрасположенность. 90% пациентов с ревматоидным артритом являются носителями специфического гена HLA-DR1 или DR4.
В 40% случаев провоцировать начало ревматоидного артрита или его обострения могут респираторные инфекции – грипп и ангина. Также предрасполагающими факторами считают травмы, переохлаждения, эмоциональные и физические переутомления.
Патогенез
Заболевание имеет аутоиммунный характер. Это означает, что воспалительный процесс в суставах вызван воздействием собственных антител, распознающих свои клетки как чужеродные антигены.
Первичное воспаление начинается в синовиальной оболочке сустава. Сюда проникают антитела и клетки, вырабатывающие биологически активные вещества, способствующие воспалению. Постепенно эти вещества накапливаются и воспалительный процесс захватывает все большую площадь суставной оболочки.
В патогенезе ревматоидного артрита задействованы все компоненты иммунной системы человека, однако наибольшее значение имеет нарушение функции Т-и В-лимфоцитов. Также патогенез ревматоидного артрита в значительной степени обусловлен фактором некроза опухоли (ФНО). Это вещество запускает все аутоиммунные процессы в организме. Избыточный синтез ФНО способствует переходу острого воспаления в хроническое.
В итоге схема формирования ревматоидного артрита выглядит следующим образом:
- В-лимфоциты под влиянием нарушений в иммунной системе вырабатывают измененный иммуноглобулин;
- В ответ на это плазматическими клетками суставной оболочки вырабатывается ревматоидный фактор;
- В результате соединения ревматоидного фактора и иммуноглобулина образуются иммунные комплексы, которые оседают в соединительной ткани;
- Развивается воспалительный и дегенеративный процесс.
Максимальные изменения наблюдаются именно в суставной оболочке, которая быстро увеличивается в объеме и разрушает хрящ и подлежащую кость. Прогрессирование иммунных нарушений приводит к поражению не только суставов, но и внутренних органов.
Механизм повреждения тканей выглядит следующим образом:
- Отек синовиальной оболочки, накопление в ней лимфоцитов;
- Разрастание синовиальной ткани;
- Разрастание капилляров;
- Отложение фибрина на синовиальной оболочке;
- Уплотнение мягких тканей;
- Деформация сустава;
- Образование контрактур и анкилозов – неподвижных соединений.
Исходом становится полное нарушение функции сустава.

Симптомы
Начинается ревматоидный артрит с симметричного поражения мелких суставов – пальцы рук и стоп. Основной жалобой пациентов становится боль – наиболее выраженная по утрам и ослабевающая к вечеру. У некоторых пациентов перед суставными болями наблюдаются мышечные. На ранней стадии симптоматика ревматоидного артрита неспецифична, что затрудняет постановку диагноза.
У некоторых пациентов после дебюта заболевания формируется ремиссия с полным исчезновением симптомов. Однако через некоторое время болезнь возвращается, поражая большее количество суставов.
По мере прогрессирования ревматоидного артрита развивается воспаление более крупных суставов. Сначала боли возникают только при движениях, а затем и в покое. Изменяется и внешний вид сустава. Наблюдается покраснение и отечность кожи над ним, отмечается ограничение движений.
Главным клиническим признаком ревматоидного артрита является утренняя скованность. Она возникает из-за нарушения функции надпочечников и скопления жидкости в полости сустава.
Диагностическую значимость симптом утренней скованности имеет в том случае, если она продолжается более часа.
Ограничение объема активных и пассивных движений обусловлено болевым синдромом и образующимися мышечными контрактурами.
В клинике ревматоидного артрита есть такие понятия, как суставные деформации и девиации, анкилозы.
Девиация. Это образование угла между смежными костями из-за вывихов и подвывихов. Наиболее частой девиацией является ульнарная – отклонение пальцев руки в сторону локтя. Кисть в этом случае называют «плавник моржа».
Деформация. Обусловлена мышечными контрактурами. Наиболее частой деформацией при ревматоидном артрите является «шея лебедя» — палец приобретает форму лебединой шеи или крючка.
Анкилоз. Это срастание костных поверхностей сустава в результате разрушения хрящевой прокладки между ними.
Такие деформации приводят к тому, что сустав не выполняет свою функцию. Человек не способен выполнять профессиональные и даже бытовые действия.
С самого начала болезни проявляются и системные признаки. Человек быстро теряет в весе – за полгода возможно снижение массы тела на 20 кг. Наблюдается умеренная лихорадка, общее недомогание, повышенная утомляемость.

Выделяют несколько системных признаков болезни:
- Часто поражаются мышцы – сначала человека беспокоят мышечные боли, затем развивается воспаление с очагами некроза. Постепенно формируется мышечная атрофия;
- Поражение кожи. Для ревматоидного артрита характерны сухость и шелушение кожи, подкожные кровоизлияния. В области нижних третей голеней появляются геморрагические высыпания. У 70% пациентов отмечается похолодание кистей и стоп;
- Ревматоидные узелки. Характерный признак артрита. Узелки представляют собой округлые безболезненные образования диаметром до 3 см. Они образуются на разгибательных поверхностях пальцев, локтей, коленей. Узелки обычно появляются в период обострения;
- Ревматоидный васкулит. Наблюдается у 20% пациентов, в основном у мужчин. Проявляется геморрагическими высыпаниями на коже и слизистых, поражением внутренних органов;
- Лимфаденопатия. Наблюдается у 60% пациентов. Страдают все группы периферических лимфоузлов. Они увеличиваются в размере до 3 см, подвижны и безболезненны;
- Анемия. Наблюдается у 50% больных с ревматоидным артритом. Проявляется характерными симптомами железодефицита — сухость кожи, ломкость волос и ногтей, слабость, обморочные состояния;
- Поражение почек. Встречается в 25% случаев. Развивается гломерулонефрит и амилоидоз.
Диагностика
Диагностика ревматоидного артрита включает клиническое обследование пациента и проведение лабораторно-инструментальных методов:
- Исследование крови. Обнаруживается снижение гемоглобина и эритроцитов. При длительном течении заболевания отмечается снижение лейкоцитов. Характерно повышение эозинофилов и тромбоцитов;
- Ревматоидный фактор. В зависимости от наличия или отсутствия этого фактора выделяют два типа артрита – серопозитивный и серонегативный;
- Исследование синовиальной жидкости. Изменяется ее вязкость, жидкость становится мутной из-за выпадающих нитей фибрина;
- Рентгенологическое исследование. Позволяет определить стадию заболевания – в зависимости от степени поражения хряща и костной ткани;
- Компьютерная и магнитно-резонансная томография. Наиболее точные методы диагностики.

Последствия
Так как ревматоидный артрит является хроническим и постепенно прогрессирующим заболеванием, неизбежно развитие осложнений. Они связаны как с самим заболеванием, так и с проводимой терапией:
- Амилоидоз. Поражаются почки и желудочно-кишечный тракт. В первом случае формируется почечная недостаточность, во втором — развивается упорная диарея, приводящая к потере массы тела;
- Остеопения. Снижается прочность костной ткани, в результате повышается риск развития переломов;
- Неходжкинские лимфомы. Это опухоли лимфоидной ткани, развивающиеся у 2% пациентов.
Отмечается снижение продолжительности жизни пациентов в среднем на 5-10 лет.
Принципы лечения
Лечение проводится консервативным методом. Принципы терапии – следующие:
- Лечебная диета;
- Прием лекарственных препаратов;
- Плазмаферез;
- Физиотерапия.
Хирургическое лечение используется при выраженных деформациях суставов.
Ревматоидный артрит – заболевание с неуточненной этиологией. В основе патогенеза болезни лежит аутоиммунный воспалительный процесс, поражающий сперва синовиальную оболочку сустава, а затем и внутренние органы. Основными симптомами являются боли и нарушение функции суставов. Причиной инвалидности становится необратимая суставная деформация.
83. Ревматоидный артрит: этиология, патогенез, классификация, клиника, диагностика, течение, исходы, лечение.
Ревматоидный артрит (РА) – хроническое системное аутоиммунное заболевание соединительной ткани с преимущественным поражением суставов по типу эрозивно-деструктивного прогрессирующего полиартрита.
Синдром Фелти – вариант РА, включающий хронический полиартрит, спленомегалию, лейкопению.
Эпидемиология: заболеваемость 0,5-1 % населения, пик заболеваемости – 5-ое десятилетие жизни; самое инвалидизирующее поражение суставов – через 10 лет от начала болезни инвалидами являются 50% больных, через 20 лет – все 100%.
Этиология неизвестна, обсуждают участие следующих факторов:
а) генетическая предрасположенность (коррелирует с HLA DR4, Dw4 и др. антигенами HLA)
б) инфекционные агенты (на роль этиологического фактора предендуют вирус Эпстайна-Барра (повышенные титры к нему выявляются у 80% больных), ретровирусы, вирусы краснухи, герпеса, микоплазмы, микобактерии)
1. В основе – генетически детерминированные аутоиммунные процессы, возникающие из-за дефицита Т-супрессорной функции лимфоцитов под влиянием неизвестного этиологического фактора. В дебюте процесса характерна АГ-специфическая активация Т-хелперов с гиперпродукцией провоспалительных (ФНО – важнейший фактор, ИЛ-1, ИЛ-8 и др.) и относительным дефицитом противовоспалительных (ИЛ-4 и др.) медиаторов, стимуляция В-лимфоцитов синовии с синтезом ревматоидного фактора – измененного IgМ, иногда IgG или IgA к фрагменту IgG собственных тканей (является аутоантигеном)
2. Повреждение сустава начинается с воспаления синовиальной оболочки (синовита), продуцирующей синовиальную жидкость, затем из-за аутоиммунного воспаления формируется панус – грануляционная ткань, происходящая из воспаленной синовиальной оболочки, состоящая из активно пролиферирующих фибробластов, макрофагов, лимфоцитов и очень богатая сосудами; панус интенсивно растет, прорастает в хрящ и разрушает его с помощью ряда ферментов
3. Хрящ постепенно разрушается и исчезает, происходит его замена грануляционной тканью с развитием анкилоза, деформации сустава, формированием эрозий костей (узур), воспалением околосуставных тканей.
а) по степени серопозитивности: серопозитивный и серонегативный
б) по степени активности: минимальной, средней, высокой
в) по данным рентгенографии суставов: I – околосуставной остеопороз, II – остеопороз + незначительное сужение суставной щели, могут быть единичные узуры, III – остеопороз + резкое сужение суставной щели + множественные узуры, IV – остеопороз + сужение суставной щели + множественные узуры + могут быть костные анкилозы
г) в зависимости от функциональной недостаточности сустава: 0 – отсутствует, I – ограничение профессиональной трудоспособности, II – утрата профессиональной трудоспособности, III – утрата способности к самообслуживанию
– за несколько недель-месяцев РА может предшествовать продромальный период (недомогание, усталость, депрессия и др.)
а) суставной синдром
– заболевание начинается чаще всего подостро с постепенного нарастания боли и скованности в мелких периферических суставах (лучезапястных, пястнофаланговых, проксимальных межфаланговых, голеностопных, плюснефаланговых); практически никогда не поражаются суставы позвоночника, дистальные межфаланговые суставы и суставы большого пальца стопы, проксимального межфалангового сустава мизинца (суставы-исключения)
– поражение суставов двустороннее, симметричное (воспалительный синовит)
– боль в области суставов длительная, усиливающаяся при нагрузках и уменьшающаяся ночью, утром выражена сильнее, чем вечером
– утренняя скованность суставов более 1 часа (причины: смещение в дневную сторону пика секреции ГКС и индукция воспаления ИЛ-6, пик синтеза которого происходит в ночное время)
– характерны воспалительные изменения мелких периферических суставов: повышение температуры кожи, отек, однако кожа над суставами не гиперемирована
– атрофии межкостных мышц тыла кистей, амиотрофии других мышц вблизи пораженных суставов
– в конечном итоге процесс деструкции в суставах ведет к анкилозу, деформации, контрактурам и затуханию воспаления («ревматоидная кисть»: отклонение пальцев в локтевую сторону – «плавник моржа»; сгибание пальцев в пястно-фаланговых и переразгибание в дистальных межфаланговых суставах –«бутоньеркя»; сгибание пальцев в пястно-фаланговых и дистальных межфаланговых и переразгибание в проксимальных межфаланговых суставах – «шея лебедя»; сгибательная и вальгусная деформация коленного сустава и др.)
б) внесуставные проявления РА:
– конституциональные: слабость, недомогание, похудание, субфебрильная температура
– ревматоидные узелки – скопления иммунных комплексов над пораженными суставами или в области разгибательной поверхности локтевой кости; размеры узелков от 2-3 мм до 4-5 см, безболезненные, могут быть как подвижными (располагаются в подкожной клетчатке), так и неподвижными (располагаются под подкожной клетчаткой)
– сердечно-сосудистые: перикардит, «ранний атеросклероз», дигитальный артериит (вплоть до синдрома Рейно)
– легочные: сухой плеврит, интерстициальный фиброз легких
– поражения НС: компрессионная нейропатия (сдавление нервных стволов из-за деформации суставов), симметричная нейропатия, множественный мононеврит (поражение vasa nervorum), цервикальный миелит
– почечные: амилоидоз, почечный канальцевый ацидоз, интерстициальный нефрит (чаще из-за ЛС)
– гематологические: анемия, умеренный лейкоцитоз, тромбоцитоз; нейтропения при синдроме Фелти
Варианты течения РА:
а) медленно прогрессирующий – даже многолетнее существование РА не приводит к тяжелым нарушениям суставов, повреждение суставных поверхностей развивается медленно, долго сохраняется функция суставов
б) быстро прогрессирующий – высокая активность процесса с образованием костных эрозий, деформаций суставов или вовлечением внутренних органов в течение первого года болезни
в) без заметного прогрессирования – слабо выраженный полиартрит с незначительной, но стойкой деформацией мелких суставов кистей; лабораторные признаки активности практически не выражены
В исходе РА: потеря функции пораженных суставов (из-за деформации, анкилозов, контрактур).
1. Лабораторные исследования:
а) ОАК: умеренная нормохромная анемия, умеренный лейкоцитоз, тромбоцитоз, повышенная СОЭ в период активности заболевания
б) БАК: повышение общего белка, диспротеинемия (умеренная гипоальбуминемия, гипергаммаглобулинемия), увеличение СРБ в периода активности заболевания
в) иммунограмма: ревматоидный фактор (у 80% больных, однако он неспецифичен, выявляется у пожилых и в норме, при при аутоиммунном гепатите и тиреоидите, СКВ, СС, ДМ, при вирусных и бактериальных инфекциях, инфекционном эндокардите, саркоидозе), антинуклеарные антитела (у 40-80%, более специфичны для СКВ); снижение количества Т-лимфоцитов, Т-супрессорной функции, дисиммуноглобулинемия; ЦИК (у 30-50%)
2. Инструментальные исследования:
а) рентгенография суставов – околосуставной эпифизарный остеопороз (крупнопетлистая костная структура, истончение и подчеркнутость контуров кортикального слоя, исчезновение постепенного перехода от серого тона губчатого вещества к более светлому контуру кортикального слоя, «размытость» трабекулярного рисунка эпифиза), сужение суставной щели, краевые эрозии (узуры)
б) радиоизотопное исследование суставов с 99 Тс (незначительно включается в неизмененную синовию, при развитии в ней воспаления концентрация изотопа значительно возрастает)
в) биопсия синовиальной оболочки (гипертрофия и увеличение количества ворсинок, пролиферация покровных синовиальных клеток, отложение фибрина на поверхности синовии, очаги некроза)
г) исследование синовиальной жидкости (при РА – мутная, вязкость снижена, количество клеток в мкл 5-25 тыс., нейтрофилов > 75%, мононуклеаров 300 ЕД, выявляется РФ)
Диагностические критерии РА:
Для постановки диагноза РА необходимо наличие по крайне мере 4-х критериев из следующих:
1. утренняя скованность более 1 часа
2. артрит ≥ 3 суставов (полиартрит)
3. артрит суставов кистей
4. симметричный артрит
5. ревматоидные узлы
6. ревматоидный фактор
7. характерные рентгенологические изменения
Эти признаки должны длиться по крайней мере 6 недель, т.к. иногда другие артриты могут проявляться так же.
1. Лечение должно быть постоянным (всю жизнь), комплексным (медикаментозное + физиотерапевтическое + санаторно-курортное + хирургическое по показаниям), индивидуальным, этапным.
2. Медикаментозная терапия:
А. Базисная терапия (медленно действующие препараты):
– арава (лефлюнамид) (1-е место по эффективности, применяется > 5 лет)
– метотрексат (2-е место по эффективности, применяется > 20 лет)
– препараты золота (тауредон) (3-е место по эффективности, применяется > 60 лет)
– сульфасалазин (4-е место по эффективности, применяется > 50 лет)
– D-пеницилламин (5-е место по эффективности, применяется > 40 лет)
– азатиоприн (6-е место по эффективности, применяется > 30 лет)
– аминохинолиновые препараты (плаквенил) (7-е место по эффективности, применяется > 40 лет);
Все эти препараты эффективны в 40% случаев, в 30% – побочные эффекты, еще в 30% – нет никакого эффекта; в среднем эффект от базисной терапии наступает через 2 месяца (арава – 1 месяц). Возможно комбинировать базисные препараты (метотрексат + сульфасалазин + плаквенил и др.), но только в случае их патогенетической сочетаемости.
Б. Противовоспалительная терапия:
1) НПВС: традиционные, классические (индометацин, диклофенак 75-150 мг/сут в 2-3 приема, ибупрофен 1,2-3,2 г/сут в 3-4 приема и др.) и селективные ингибиторы ЦОГ-2 (меньше побочных эффектов: мелоксикам / мовалис 7,5-15 мг/сут, нимесулид / нимесил / найз 100 мг/сут в 2 приема, целекоксиб / целебрекс)
– назначить можно любой препарат, обычно начинают с классических, при наличии противопоказаний (язва желудка и ДПК, АГ, заболевания почек) показаны селективные ингибиторы ЦОГ-2 (с них не начинают из-за более высокой стоимости данных ЛС)
– если эффекта нет, препарат меняют (эффективность оценивается уже через 5-7 дней использования)
– основной побочный эффект: поражение ЖКТ в виде диспепсии или язвы (желудка, 12ПК, кишечника); при опасности язв можно использовать ингибиторы протонной помпы (омепразол)
2) ГКС – могут применяться
а) внутрь в малых дозах: 5-7,5 мг преднизолона
б) в/в в виде пульс-терапии – только при наличии системных проявлений (кроме амилоидоза почек)
в) внутрисуставно (не > 3 раз/год) – при синовите: дипроспан (бетаметазон), депо-медрол (метилпреднизолон), кеналог (триамцинолон)
Каждому больному должно быть назначено минимум 2 препарата (1 – из А, 1 – из Б), но может быть и больше. Только у 20% больных удается достичь ремиссии заболевания (на каком-то базисном препарате), вторично он уже не эффективен. Все больные РА имеют право на бесплатное амбулаторное лечение, но в приказ включены не все препараты (нет аравы: месяц – 100$ или препаратов золота: месяц – 70$).
Современные тенденции в лечении РА – анти-ФНОα-терапия: Etanercept (Immunex, Enbrel) – растворимый димер ФНОα-рецептора, соединенный с IgG1 (п/к по 2,5 мг 2 раза в неделю), Infliximab (Remicade) – моноклональное антитело против ФНОα (в/в капельно через 8 недель); стоимость годичного курса лечения – 10000-12000$, эти препараты высокоэффективны, т.к. останавливают прогрессирование РА.
3. Физиотерапевтическое лечение – должно быть направлено на уменьшение боли и воспаления, нельзя тепловые процедуры (грязи, озокерит, парафин), можно электро-, лазеро-, бальнеотерапию.
4. Санаторно-курортное лечение: рекомендованы санатории «Радон» (Дятловский район Гродненской области), «Приднепровский» (Рогачевский район); «Им. Ленина» (г. Бобруйск)
5. Хирургическое лечение:
а) синовэктомия – вызывает затухание процесса только на 2-3 года, т.е. временно; в настоящее время
не используется, т.к. вызывает вторичный артрит
б) протезирование суставов (тазобедренного, коленного и более мелких)
6. Реабилитация: изменение стереотипа двигательной активности для профилактики деформации суставов; ортопедические пособия, удерживающие сустав в правильном положении; лечебная физкультура, ФТЛ, санаторно-курортное лечение.
В ревматологии хронические воспалительные изменения в суставах представляют обширную группу заболеваний. Одним из наиболее часто встречающихся, считается ревматоидный артрит (РеА). Это хронический недуг, имеющее системный характер, причина которого до сих пор не установлена. Патогенез ревматоидного артрита сложен и имеет ряд отличительных особенностей. О симптомах ревматоидного артрита читайте в прошлой статье. Поражение соединительной ткани и эрозивно-деструктивный характер повреждений приводят к нарушениям функции суставов, формированию контрактур, невозможности выполнять обычные движения. Системность болезни заключается в том, что кроме хрящевых поверхностей сочленений воспаление, обусловленное патогенезом, развивается во всех внутренних органах организма.
Роль аутоиммуных процессов в развитиии ревматоидного артрита
В патогенезе ревматоидного артрита ведущую роль играет состояние иммунной системы. Причины развития ревматоидного артрита до настоящего времени неизвестны. Выдвигается множество гипотез о влиянии на этиологию артрита инфекционных агентов, переохлаждения, травм и т.д. Но большинство исследователей склоняются к тому, что все вышеперечисленное является лишь толчком к патогенезу патологического аутоиммунного процесса.
К факторам риска РеА относят:
- лиц женского пола в возрасте старше пятидесяти лет;
- людей, имеющих родственников, больных РеА;
- лиц с наличием определенных антигенов гистосовместимости по НLА – системе;
- наличие врожденной патологии опорно-двигательного аппарата и соединительной ткани.
В норме лимфоцитарная система выполняет защитную функцию, реагируя на попадание в организм чужеродных белков – антигенов и вырабатывая специфические иммуноглобулины, способствующие уничтожению посторонних вредоносных клеток. Но в патогенезе РеА механизм иммунного ответа отказывается нарушенным. Таким образом, в основе патогенеза ревматоидного артрита лежит сбой в распознавании чужих и своих клеток, обусловленный как наследственными факторами, так и дефектом, возникшим под влиянием предрасполагающих внешних факторов (инсоляции, нарушений обмена, стрессов и пр.). Подробнее о грамотной дифференциальной диагностике ревматоидного артрита можно прочитать здесь.
Патогенез РеА обуславливает то, что начало выглядит не как артритические нарушения, а как системный васкулит. Воздействие неизвестного антигена активизирует макрофаги и В-лимфоциты, которые вырабатывают антитела – иммуноглобулины класса G. В свою очередь Т-лимфоциты воспринимают эти антитела, как агрессивные, чужеродные и, пытаясь их уничтожить, вырабатывают большое количество биологически активных веществ (цитокины, интерлейкины и т.д.). Под действием этих веществ усиливается проницаемость сосудистой стенки за счет поражения мелких кровеносных сосудов, возникает отек, активируются клетки синовиальной оболочки (фибробласты, остеокласты, макрофаги), которые играют в патогенезе огромную роль и вызывают разрастание лимфоидной ткани, разрушение кости и хряща, усиливают и поддерживают воспаление в суставе.
Ревматоидный фактор
Аутоантитела, образующиеся на собственные клетки, носят название ревматоидного фактора (РФ). Это специфические вещества, по наличию которых и определяют ревматоидный артрит. В патогенезе важную роль имеют иммунные комплексы – это сцепленные вместе иммуноглобулины и аутоантитела. Они не могут быть переварены макрофагами и выведены из организма, поэтому оседают на поверхности синовиальной оболочки, сосудистой стенки, а других тканях поддерживая активность воспалительного процесса. Важным в патогенезе хронического течения имеет то, что образование иммунных комплексов стимулирует нарушение микроциркуляции, формирование микроскопических тромбов в сосудах, разрушение клеток, продукты распада которых вновь воспринимаются как чужеродные антитела. Таким образом, замыкается порочный круг и наступает хронизация воспаления. Важную роль в патогенезе отводят гуморальному звену – большое количество образующихся интерлейкинов, фактора некроза опухоли, гистамина вызывают реакцию по типу аллергической и способствуют системным проявлениям.
Клиническая картина
Исходя из патогенеза РеА можно сказать, что первые изменения в суставах могут протекать незаметно. Выраженные симптомы, такие как боль, отечность, изменением температуры и цвета кожных покровов в месте поражения появляются уже на стадии развернутого воспалительного процесса. Чем сильнее иммунная аутоагрессия, тем большее количество суставов поражается, тем ярче клинические проявления.
Заболевание может поражать абсолютно все суставы, и крупные, и мелкие. Может начинаться как моноартрит – с одного сустава, а может захватывать сразу несколько. Это обусловлено патогенезом системного васкулита. Характерна утренняя скованность, невозможность сразу включится в работу, ограничение подвижности после периода длительного покоя. Описанный в патогенезе, выброс большого количества медиаторов воспаления приводит к развитию общих реакций:
- лихорадки (от субфебрилитета до гектической);
- головной боли;
- недомогания;
- потеря массы тела, связанная как со снижением аппетита, так и с обменными нарушениями;
- мышечные боли и возможная атрофия;
- анемия, тромбоцитопения;
- значительная раздражительность, апатия, депрессия.
Выраженность симптомов и острота течения, опираясь на патогенез, зависят от наличия, либо отсутствия в крови и суставной жидкости РФ. В связи с этим выделяют серопозитивную (при наличии ревматоидного фактора) и серонегативную (при его отсутствии) формы ревматоидного артрита. Серопозитивный вариант характеризуется более агрессивной иммунологической реакцией, менее благоприятным исходом, склонен к системным поражениям внутренних органов. В случае генерализованного течения в процесс вовлекается кожа (гиперкератоз, отложение иммунных комплексов в виде характерных ревматоидных узелков), сердечно-сосудистая система (миокардит, перикардит), оболочки глаз (увеит, иридоциклит, глаукома), нервная система (невриты, сакроилеиты).
Диагностические мероприятия
В связи с неспецифическими первыми проявлениями постановка правильного диагноза чрезвычайно сложна. Иногда период обследования занимает до полугода.
В диагностике применяют:
- физикальные методы (опрос, сбор анамнеза, осмотр);
- лабораторные (общие анализы крови и мочи, биохимические исследования);
- иммунологические методы;
- рентгенодиагностика;
- сопутствующие методики: ультразвуковое сканирование, осмотр глазного дна, электрокардиография и прочее.
Сбор анамнеза позволяет выявить наследственную предрасположенность и отследить заболеваемость ревматоидным артритом в семье больного. Лабораторные анализы показывают наличие и степень общей реакции организма, участвующей в патогенезе (повышение СОЭ, лейкоцитоз, наличие в крови РФ, СРБ, серомукоида, фибриногена и т.д.). Рентгенодиагностика включает в себя как обзорную рентгенографию, так и более современные методы – компьютерную томографию и магнитно-резонансный способ исследования, которые считаются более информативными, поскольку позволяют с точностью определить локализацию, степень активности, выявить стадию изменений в хряще и костях. Кроме этого МРТ позволяет увидеть изменения и в окружающих мягких тканях – бурситы, синовииты, тендениты, грыжи и т.д.
Исследования крови и внутрисуставной жидкости
Однако важнейшим методом для патогенетической диагностики являются иммунологические исследования крови и внутрисуставной жидкости. Ранее считалось, что обнаружение РФ может достоверно подтвердить диагноз. Однако далеко не у всех больных ревматоидным артритом он выявляется (серонегативный РеА), в то время как при других заболеваниях (саркоидоз, ситемная красная волчанка и т.д.) уровень его может быть достаточно высок. Поэтому подтвердить диагноз обнаружение РФ может только в случаях характерной клинической картины при соответствии симптомов разработанным критериям. По этой причине и, исходя из патогенеза болезни, важнейшими для диагностики считается обнаружение антител к циклическому цитруллинированному пептиду и вементину (АЦЦП, АМЦВ), а также специфических антител, называемых факторами некроза опухоли (ФНО) и антинуклеарных факторов. Достоверность данного метода девяносто восемь процентов, что позволяет быстро и точно поставить диагноз и начать лечение у большинства пациентов.
Лечение заболевания
Поскольку этиология ревматоидного артрита до сих пор не выяснена, то главным критерием в терапии является воздействие на патогенез болезни. К базовому лечению, основанному на патогенезе, относится несколько групп препаратов:
- цитостатики (метотрексат, сульфасалазин, азатиоприн и др.);
- препараты золота (ридаура);
- д-пеницилламин;
- ингибиторы ФНО (ремикейд, энбрел).
Все они подавляют активность Т-лимфоцитов, снижают выработку иммуноглобулинов, уменьшают продукцию биологически активных веществ (интерлейкинов, ФНО, гистамина и т.д.). Т.е. оказывают влияние на все цепочки патогенеза. Лечение иммуносупрессорами длительное, иногда пожизненное. Назначение только одного препарата часто не дает должного эффекта, особенно при агрессивных формах иммунологической реакции в развитии ревматоидного артрита. Поэтому часто возникает необходимость сочетания различных лекарственных средств. Это значительно повышает эффективность и дает возможность добиться стойкой ремиссии.
Симптоматическая терапия включает применение нестероидных противовоспалительных средств. Например, индометацин, диклофенак, немисулид, вольтарен. Которые снимают боль, уменьшают проницаемость сосудов синовиальной оболочки, оказывают жаропонижающее действие. Гормоны (преднизолон) назначают коротким курсом при неэффективности НСПВС. В качестве дополнительных методов используют физиопроцедуры: электрофорез, лазер; мануальную терапию, лечебную физкультуру. В случаях системного поражения – плазмоферез, гемосорбция, лимфоцитоферез.
Заключение
РеА – тяжелое аутоиммунное заболевание, часто приводящее к инвалидности. В основе его патогенеза лежат измененные иммунные реакции, как на клеточном, так и гуморальном уровне. Для правильности подбора лечения необходимо понимать патогенез заболевания. А также постараться воздействовать на все звенья патологического процесса. Только в этом случае удастся добиться стойкой ремиссии и предупредить инвалидность.
Ревматоидный артрит

Ревматоидный артрит – ревматический процесс, характеризующийся эрозивно-деструктивными поражениями преимущественно периферических мелких суставов. Суставные признаки ревматоидного артрита включают симметричное вовлечение суставов стоп и кистей, их деформирующие изменения. К внесуставным системным проявлениям относятся серозиты, подкожные узелки, лимфаденопатия, васкулиты, периферическая нейропатия. Диагностика включает оценку клинических, биохимических, рентгенологических маркеров. Лечение ревматоидного артрита требует длительных курсов НПВП, кортикостероидов, базисных средств, иногда – хирургического восстановления суставов. Заболевание часто приводит к инвалидности.
МКБ-10

Общие сведения
Ревматоидный артрит (РА) – иммуновоспалительное поражение соединительной ткани, протекающее с суставной и внесуставной симптоматикой. Заболеваемость в популяции составляет около 1%, при этом среди женщин РА встречается в 2,5 раза чаще, чем среди мужчин. Пик развития патологии приходится на возраст от 40 до 50 лет. Ревматоидный артрит протекает хронически, а изменения суставов неуклонно прогрессируют, неизбежно приводя к инвалидности через 10-20 лет.

Причины РА
Причины, обусловливающие развитие ревматоидного артрита, достоверно не установлены. Определена наследственная природа нарушений иммунологических ответов и роль инфекционных этиофакторов (вируса Эпштейн-Барра, ретровируса, цитомегаловируса, микоплазмы, вируса герпеса, краснухи и др.).
Основу патогенеза ревматоидного артрита составляют аутоиммунные реакции, развивающиеся в ответ на действие неизвестных этиологических факторов. Эти реакции проявляются цепочкой взаимосвязанных изменений – воспалением синовиальной мембраны (синовитом), формированием грануляционной ткани (паннуса), ее разрастанием и проникновением в хрящевые структуры с разрушением последних. Исходом ревматоидного артрита служит развитие анкилоза, хронического воспаления параартикулярных тканей, контрактуры, деформации, подвывихи суставов.
Классификация
По клинико-анатомическим особенностям различают формы ревматоидного артрита:
- протекающие по типу полиартрита, олиго- или моноартрита;
- характеризующиеся системной симптоматикой;
- сочетающиеся с диффузными заболеваниями соединительной ткани, деформирующим остеоартрозом, ревматизмом;
- особые формы (ювенильный артрит, синдромы Стилла и Фелти)
По иммунологическим характеристикам выделяют серопозитивные варианты ревматоидного артрита и серонегативные, которые различаются выявлением или отсутствием ревматоидного фактора в сыворотке и суставной жидкости.
Динамика течения ревматоидного артрита может быть различной. Стремительно прогрессирующему варианту свойственна высокая активность: эрозирование костных тканей, деформирование суставов, системные поражения в течение 1-го года заболевания. Медленно развивающийся ревматоидный артрит даже многие годы спустя не вызывает грубых морфологических и функциональных изменений суставов, протекает без системного вовлечения.
По активности клинико-морфологических изменений дифференцируют три степени ревматоидного артрита.
- I ст. При минимальной активности процесса отмечаются незначительные боли в суставах, преходящая скованность в утренние часы, отсутствие локальной гипертермии.
- II ст. Ревматоидный артрит средней активности характеризуется болями в покое и в движении, многочасовой скованностью, болевым ограничением подвижности, стабильными экссудативными явлениями в суставах, умеренной местной гипертермией кожи.
- III ст. Для высокой активности ревматоидного артрита типична сильная артралгия, выраженная экссудация в суставах, гиперемия и припухлость кожи, непроходящая скованность, резко ограничивающая подвижность.
По степени нарушения опорных функций при ревматоидном артрите различают стадии ФН I, ФН II и ФН III.
- Функциональные нарушения I ст. характеризуются минимальными двигательными ограничениями с сохранением профессиональной пригодности.
- На стадии ФН II подвижность суставов снижена резко, развитие стойких контрактур ограничивает самообслуживание и ведет к утрате работоспособности.
- Стадия ФН III ревматоидного артрита определяется тугоподвижностью или тотальной неподвижностью суставов, потерей возможности самообслуживания и необходимостью постоянного ухода за таким пациентом.
Симптомы ревматоидного артрита
Суставные проявления
Доминирующим в клинике ревматоидного артрита является суставной синдром (артрит) с характерным двусторонним симметричным вовлечением суставов. На продромальном этапе отмечается усталость, периодические артралгии, астения, потливость, субфебрилитет, утренняя скованность. Дебют ревматоидного артрита обычно связывается пациентами со сменой метеофакторов, сезонов года (осени, весны), физиологических периодов (пубертатного, послеродового, климактерического). Провоцирующей причиной ревматоидного артрита может служить инфекция, охлаждение, стресс, травма и др.
При остром и подостром дебюте ревматоидного артрита наблюдается лихорадка, резкая миалгия и артралгия; при малозаметном прогрессировании – изменения нарастают длительно и не сопровождаются существенными функциональными нарушениями. Для клиники ревматоидного артрита типично вовлечение суставов стоп и кистей, запястий, коленных и локтевых суставов; в отдельных случаях поражение касается тазобедренных, плечевых и суставов позвоночника.
Объективные изменения при ревматоидном артрите включают скопление внутрисуставного экссудата, отечность, резкую пальпаторную болезненность, двигательные ограничения, локальную гиперемию и гипертермию кожи. Прогрессирование ревматоидного артрита ведет к фиброзированию синовиальной мембраны и периартикулярных тканей и, как следствие, к развитию деформирования суставов, контрактур, подвывихов. В исходе ревматоидного артрита наступает анкилозирование и обездвиженность суставов.
При поражении синовиальных влагалищ сухожилий кисти – теносиновите нередко развивается синдром запястного канала, патогенетическую основу которого составляет невропатия срединного нерва в результате его сдавления. При этом отмечается парестезия, снижение чувствительности и подвижности среднего, указательного и большого пальцев кисти; боль, распространяющаяся на все предплечье.
Внесуставные поражения
Развитие внесуставных (системных) проявлений более характерно для серопозитивной формы ревматоидного артрита тяжелого длительного течения. Поражение мускулатуры (межкостной, гипотенара и тенара, разгибателей предплечья, прямой бедренной, ягодичной) проявляется атрофией, снижением мышечной силы и тонуса, очаговым миозитом. При вовлечении в ревматоидный артрит кожных покровов и мягких тканей появляется сухость и истонченность эпидермиса, геморрагии; могут возникать мелклочаговые некрозы подногтевой области, приводящие к гангрене дистальных фаланг. Нарушение кровоснабжения ногтевых пластин ведет к их ломкости, исчерченности и дегенерации.
Типичными признаками ревматоидного артрита служат подкожно расположенные соединительнотканные узелки диаметром 0,5-2 см. Для ревматоидных узелков характерна округлая форма, плотная консистенция, подвижность, безболезненность, реже – неподвижность вследствие спаянности с апоневрозом. Эти образования могут носить единичный или множественный характер, иметь симметричную либо несимметричную локализацию в области предплечий и затылка. Возможно образование ревматоидных узелков в миокарде, легких, клапанных структурах сердца. Появление узелков связано с обострением ревматоидного артрита, а их исчезновение – с ремиссией.
Наиболее тяжелым течением ревматоидного артрита отличаются формы, протекающие с лимфоаденопатией, поражением ЖКТ (энетритами, колитами, амилоидозом слизистой прямой кишки), нервной системы (нейропатией, полиневритом, функциональными вегетативными нарушениями), вовлечением органов дыхания (плеврит, диффузный фиброз, пневмонит, фиброзирующий альвеолит, бронхиолит), почек (гломерулонефрит, амилоидоз), глаз. Со стороны магистральных сосудов и сердца при ревматоидном артрите могут возникать эндокардит, перикардит, миокардит, артериит коронарных сосудов, гранулематозный аортит.
При ревматоидных висцеропатиях вследствие панартериита отмечаются кожные симптомы в виде полиморфной сыпи и изъязвлений; геморрагический синдром (носовые, маточные кровотечения), тромботический синдром (мезентериальные тромбозы).
Осложнения
Тяжкими осложнениями, обусловленными ревматоидным артритом, могут служить поражения сердца (инфаркт миокарда, митральная и аортальная недостаточность, аортальный стеноз), легких (бронхоплевральные свищи), хроническая недостаточность почек, полисерозиты, висцеральный амилоидоз.
Диагностика
Подозрение на ревматоидный артрит является показанием для консультации ревматолога. Исследование периферической крови выявляет анемию; нарастание лейкоцитоза и СОЭ напрямую связано с активностью ревматоидного артрита. Типичными иммунологическими маркерами при ревматоидном артрите служат выявление РФ, снижение числа Т-лимфоцитов, повышение криоглобулинов, обнаружение антикератиновых антител (АКА). Объективное подтверждение получают с помощью:
- Рентгенографии. К рентгенологическим критериям ревматоидного артрита относится обнаружение диффузного или пятнистого эпифизарного остеопороза, сужения суставных щелей, краевых эрозий. По показаниям назначается МРТ сустава.
- Биопсии и пункции сустава. Для взятия образца внутрисуставной жидкости производят пункцию сустава. При микроскопии суставной жидкости обнаруживаются неспецифические воспалительные признаки. Исследование биоптата синовиальных мембран при ревматоидном артрите демонстрирует гипертрофию и увеличение числа ворсинок; пролиферацию плазматических, лимфоидных и покровных клеток (синовиоцитов) суставных оболочек; фибриновые отложения; зоны некроза.

Лечение ревматоидного артрита
В основе терапии при ревматоидном артрите лежит назначение курса быстродействующих (противовоспалительных) и базисных (модифицирующих течение заболевания) препаратов, проведение эфферентной терапии, лечебной физкультуры. При необходимости выполняются хирургические вмешательства.
- Фармакотерапия. К группе быстродействующих относятся НПВС (диклофенак, ибупрофен, напроксен), кортикостероиды, купирующие воспаление и боль. Использование базисных препаратов (сульфасалазина, гидроксихлороквина метотрексата, лефлуномида) позволяет достичь ремиссии ревматоидного артрита и предотвратить/замедлить дегенерацию суставов.
- Гравитационная хирургия крови. Кроме приема медикаментов, при ревматоидном артрите показано проведение экстракорпоральной гемокоррекции – криоафереза, мембранного плазмафереза, экстракорпоральной фармакотерапии, каскадной фильтрации плазмы.
- Лечебная физкультура. Пациентам с ревматоидным артритом рекомендуются занятия ЛФК, плавание.
- Ортопедические операции. С целью восстановление функции и структуры суставов применяются хирургические вмешательства – артроскопия, эндопротезирование разрушенных суставов.
Экспериментальное лечение
К относительно новым препаратам, использующимся в лечении ревматоидного артрита, относятся биологические средства, блокирующие провоспалительный белок-цитокин – фактор некроза опухоли (этанерсепт, инфликсимаб, адалимумаб). Препараты-инактиваторы ФНО вводятся в форме инъекций и назначаются в комбинации с базовыми препаратами. Перспективной и многообещающей методикой лечения ревматоидного артрита является терапия стволовыми клетками, направленная на улучшение трофики и регенерацию суставов.
Прогноз и профилактика
Изолированное, локализующееся в 1-3-х суставах, не резко выраженное воспаление при ревматоидном артрите позволяет надеяться на благоприятный прогноз. К отягощающим перспективу заболевания факторам относятся полиартрит, выраженное и резистентное к терапии воспаление, наличие системных проявлений. Ввиду отсутствия превентивных методов, возможна лишь вторичная профилактика ревматоидного артрита, которая включает предупреждение обострений, диспансерный контроль, подавление персистирующей инфекции.
Ревматоидный артрит: клиника, диагностика, лечение
Ревматоидный артрит — системное заболевание соединительной ткани с преимущественным поражением мелких суставов по типу эрозивно-деструктивного полиартрита неясной этиологии со сложным аутоиммунным патогенезом.
Причины заболевания на сей день неизвестны. Косвенные данные, такие, как увеличение количества лейкоцитов в крови и скорости оседания эритроцитов (СОЭ), указывают на инфекционную природу процесса. Полагают, что заболевание развивается в результате инфекции, вызывающей нарушения иммунной системы у наследственно предрасположенных лиц; при этом образуются т. н. иммунные комплексы (из антител, вирусов и проч.), которые откладываются в тканях и приводят к повреждению суставов. Но неэффективность лечения РА антибиотиками скорее всего свидетельствует о неправильности такого предположения.
Лечение сосредотачивается в основном на облегчении боли, замедлении развития заболевания и восстановлении повреждений с помощью хирургического вмешательства. Раннее обнаружение заболевания с помощью современных средств может значительно сократить вред, который может быть нанесён суставам и другим тканям.
Впервые может проявиться после тяжёлой физической нагрузки, эмоционального шока, утомления, в период гормональной перестройки, воздействия неблагоприятных факторов или инфекции.Содержание
Как и для большинства аутоиммунных заболеваний, здесь можно выделить 3 основных фактора (ревматологическая триада):
1. Наследственная склонность к аутоиммунным реакциям.
2. Инфекционный фактор Гипотетические триггеры ревматических заболеваний
— парамиксовирусы — вирусы паротита, кори, респираторно-синцитиальной инфекции
— гепатовирусы — вирус гепатита В
— герпесвирусы — вирусы простого герпеса, опоясывающего лишая, Цитомегаловирус, вирус Эпштейна-Барр (значительно выше в синовиальной жидкости * больных РА)
— ретровирусы — Т-лимфотропный вирус
3. Пусковой фактор (переохлаждение, гиперинсоляция, интоксикации, мутагенные медикаменты, эндокринопатии, стрессы и т. д.). Для женщин длительность кормления грудью снижает вероятность развития РА. Кормление грудью в течение 24 месяцев и дольше понижает риск развития РА вдвое.
Ревматоидный артрит прогрессирует в трёх стадиях. В первой стадии происходит опухание синовиальных сумок вызывающее боль, нагрев и опухоль вокруг суставов. Вторая стадия это стремительное деление клеток которое приводит к уплотнению синовиальной оболочки. В третьей стадии, воспалённые клетки высвобождают фермент который поражает кости и хрящи, что часто приводит к деформации задетых суставов, увеличению боли и потере двигательных функций.
Как правило, вначале заболевание протекает медленно, с постепенным развёртыванием клинической симптоматики в течение нескольких месяцев или лет, значительно реже — подостро или остро. Около 2/3 случаев проявляются полиартритом, остальные — моно- или олигоартритом, причём суставной синдром часто не имеет клинической специфики, что значительно затрудняет дифференциальную диагностику. Суставной синдром характеризуется наличием утренней скованности более 30 минут и аналогичных проявлений во второй половине ночи — симптомы «тугих перчаток», «корсета»; постоянной спонтанной болью в суставах, усиливающейся при активных движениях. Исчезновение скованности зависит от активности процесса: чем больше активность, тем больше продолжительность скованности. Для суставного синдрома при ревматоидном артрите характерны монотонность, продолжительность, сохранение остаточных явлений после лечения.
Возможно наличие продромальных клинических проявлений (незначительные преходящие боли, связь боли с метеорологическими условиями, вегетативными расстройствами). Выделяют «суставы поражения» и «суставы исключения». К первым относятся (в порядке частоты встречаемости): II и III пястно-фаланговые, проксимальные межфаланговые плюснефаланговые, коленные и лучезапястные, локтевые и голеностопные. «Суставы исключения» следующие: дистальные межфаланговые, I пястно-фаланговый (большого пальца кисти).
Ревматоидный артрит часто сочетается с другими болезнями суставов — остеоартрозом, ревматизмом, системными болезнями соединительной ткани.
Выделяют следующие варианты клинического течения ревматоидного артрита:
Классический вариант (симметричное поражение как мелких, так и крупных суставов, медленнопрогрессирующее течение).
Моно- или олигоартрит с преимущественным поражением крупных суставов, чаще коленных. Выраженное начало заболевания и обратимость всех проявлений в течение 1-1,5 месяца (артралгии носят мигрирующий характер, рентгенологические изменения отсутствуют, противовоспалительные препараты дают относительно положительный эффект; в последующем возникают все симптомы, характерные для ревматоидного артрита).
Ревматоидный артрит с псевдосептическим синдромом (сопровождается лихорадкой гектического типа, ознобом, гипергидрозом, потерей веса, развитием амиотрофии, анемии, васкулитов, висцеритов; в ряде случаев клинические признаки артрита отходят на второй план).
Синдром Фелти (сочетание полиартрита и спленомегалии; возможен вариант без спленомегалии, но с лейкоцитопенией, нейтропенией, висцеритами).
Ювенильный ревматоидный артрит (начало заболевания до 16 лет):
суставно-висцеральная форма с ограниченными висцеритами.
поражение сердца, лёгких, почек, органов пищеварения;
поражение нервной системы.
Диагностика ревматоидного артрита (РА) – это процесс. Долгое время не существовало определённого теста который мог бы однозначно подтвердить наличие заболевания[источник не указан 607 дней]. В настоящее время диагностика заболевания основывается на биохимическом анализе крови, изменениями в суставах, видимых на рентгене, и на использовании основных клинических маркеров, к которым относятся: суставной синдром как таковой, а также в сочетании с общеклиническими проявлениями — лихорадкой, слабостью, потерей веса и другими[источник не указан 607 дней].
При биохимическом анализе крови исследуют СОЭ, ревматоидный фактор (ревмо-фактор), количество тромбоцитов и т.д. Наиболее прогрессивным анализом является количество антител к циклическому цитрулиновому пептиду (АЦЦП). Специфичность этого показателя составляет 97%, при этом он присутствуют в 79% сывороток от больных РА.
Диагностически важными клиническими особенностями являются отсутствие изменений цвета кожи над воспалёнными суставами, развитие тендосиновитов сгибателей или разгибателей пальцев кистей и формирование амиотрофий, типичных деформаций кистей, так называемая «ревматоидная кисть».
Критериями неблагоприятного прогноза являются:
раннее поражение крупных суставов и появление ревматоидных узелков
увеличение лимфатических узлов
вовлечение новых суставов при последующем обострении;
системный характер болезни;
персистирующая активность болезни при отсутствии ремиссии более года;
стойкое увеличение СОЭ;
раннее появление (в течение первого года) и высокие титры ревматоидного фактора
ранние (до четырёх месяцев) рентгенологические изменения со стороны поражённых суставов — быстрое прогрессирование деструктивных изменений;
обнаружение антинуклеарных антител и LE-клеток
носительство антигенов HLA-DR4; плохая переносимость базисных препаратов.
Ревматоидный артрит может начаться с любого сустава, но чаще всего начинается с мелких суставов на пальцах, руках и запястьях. Обычно поражение суставов симметрично, то есть если болит сустав на правой руке, значит должен заболеть тот же сустав на левой. Чем больше суставов поражено, тем более продвинута стадия болезни.
Другие частые симптомы:
Утренняя скованность. Обычно чем дольше длится скованность, тем активней заболевание.
Похожие на грипп симптомы, включая невысокий жар.
Боли при длительном сидении
Вспышки активности заболевания сопровождающиеся ремиссией.
Потеря аппетита, депрессия, потеря веса, анемия, холодные и/или потные ладони и ступни
Нарушение желез в районе глаз и рта, вызывающее недостаточную выработку слез и слюны.
При наличии инфекции или подозрении на неё (туберкулёз, иерсиниоз и т. п.) необходима терапия соответствующим антибактериальным препаратом. При отсутствии ярких внесуставных проявлений (например, высокой лихорадки, синдрома Фелти или палиневропатии) лечение суставного синдрома начинают с подбора нестероидных противовоспалительных средств (НПВП). Одновременно в наиболее воспалённые суставы вводят кортикостероидные препараты. Иммунокомплексная природа болезни делает показанным проведение курсов ппазмафереза, в большинстве случаев дающего выраженный эффект. Нестойкость результатов указанной терапии является показанием к присоединению так называемых базисных средств. Эти препараты действуют медленно, поэтому должны применяться не менее 6 мес, а при отчётливом положительном эффекте лечение ими обязательно продолжается и дальше (годами).
Важным моментом в лечении ревматоидного артрита является профилактика остеопороза — восстановление нарушенного кальциевого баланса в направлении повышения всасывания его в кишечнике и уменьшения выведения из организма. Необходимым компонентом в комплексе противоостеопоротических мероприятий является диета с повышенным содержанием кальция. Источниками кальция являются молочные продукты (особенно твёрдый сыр, содержащий от 600 до 1000 мг кальция на 100 г продукта, а также плавленый сыр; в меньшей степени творог, молоко, сметана), миндаль, лесные и грецкие орехи и т. д., а также препараты кальция в сочетании с витамином D или его активными метаболитами.
Важное значение в лечении имеет лечебная физкультура, направленная на поддержание максимальной подвижности суставов и сохранение мышечной массы.
Физиотерапевтические процедуры (электрофорез нестероидных противовоспалительных средств, фонофорез гидрокортизона, аппликации димексида) и санаторно-курортное лечение имеют вспомогательное значение и применяются лишь при небольшой выраженности артрита.
При стойком моно- и олигоартрите проводят синовэктомию либо введением в сустав изотопов золота, иттрия и др., либо хирургическим путём. При стойких деформациях суставов проводят реконструктивные операции.
Системная медикаментозная терапия включает применение четырёх групп препаратов:
нестероидные противовоспалительные препараты (НПВП),
Нестероидные Противовоспалительные Препараты
НПВП по-прежнему являются лечебными средствами первой линии, которые направлены, прежде всего, на купирование острых проявлений болезни, а также на обеспечение стойкой клинико-лабораторной ремиссии.
В острый период болезни используют НПВП, ГКС, пульс-терапию глюкокортикостероидами или в сочетании с цитостатическими иммунодепрессантами.
Современные НПВП оказывают выраженное противовоспалительное действие, которое обусловлено угнетением активности циклооксигеназы (ЦОГ) — ключевого фермента метаболизма арахидоновой кислоты. Особый интерес представляет открытие двух изоформ ЦОГ, которые определены как ЦОГ-1 и ЦОГ-2 и играют разную роль в регуляции синтеза простогландинов (ПГ). Доказано, что НПВП угнетают активность изоформ ЦОГ, но их противовоспалительная активность обусловлена угнетением именно ЦОГ-2.
Большинство известных НПВП подавляют прежде всего активность ЦОГ-1, чем и объясняется возникновение таких осложнений, как гастропатия, нарушение функции почек, энцефалопатия, гепатотоксичность.
Таким образом, в зависимости от характера блокирования ЦОГ, НПВП делят на селективные и неселективные ингибиторы ЦОГ-2.
Представителями селективных ингибиторов ЦОГ-2 являются мелоксикам, нимесулид, целекоксиб. Эти препараты имеют минимальный побочный эффект и сохраняют высокую противовоспалительную и анальгетическую активность. Ингибиторы ЦОГ-2 могут использоваться во всех программах лечения ревматоидного артрита, где требуется применение НПВП. Мелоксикам (Мовалис) в начале лечения при активности воспалительного процесса назначают по 15 мг/сут, а в дальнейшем переходят на 7,5 мг/сут в качестве поддерживающей терапии. Нимесулид назначается в дозе 100 мг два раза в сутки.
Целекоксиб (Целебрекс) — специфический ингибитор ЦОГ-2 — назначается по 100—200 мг два раза в сутки. Для пожилых людей подбор дозировки препарата не требуется. Однако у пациентов с массой тела ниже средней (50 кг) желательно начинать лечение с самой низкой рекомендованной дозы.
Следует избегать комбинации двух или более НПВП, поскольку их эффективность остаётся неизменной, а риск развития побочных эффектов возрастает.
Базисные препараты по-прежнему играют первостепенную роль в комплексной терапии ревматоидного артрита, но сейчас наметился новый подход к их назначению. В отличие от хорошо известной тактики постепенного наращивания терапии ревматоидного артрита («принцип пирамиды»), теперь пропагандируется раннее агрессивное лечение базисными препаратами сразу после установления диагноза, цель которого — модификация течения ревматоидного артрита и обеспечение ремиссии заболевания. Основанием для этого являются отсутствие на ранней стадии ревматоидного артрита паннуса, деформаций, остеопении, тяжёлых осложнений, сформированных аутоиммунных механизмов, высокая вероятность развития ремиссии.
Основными лекарственными средствами базисной терапии ревматоидного артрита являются: метотрексат, сульфазалазин, препараты золота, D-пеницилламин, аминохинолиновые препараты. К средствам резерва относятся циклофосфан, азатиоприн, циклоспорин А (Сандиммун). Новая группа представлена следующими препаратами: ремикейд (инфликсимаб) — химерные моноклональные антитела к фактору некроза опухоли (ФНО)-a человека; энбрел (этанерцепт) — рекомбинантные растворимые рецепторы к ФНО; тимодепрессин — селективный пептидный иммунодепрессант, действующий на уровне Т-лимфоцитов; лефлуномид (Арава) и другие.
Неэффективные на протяжении 1,5-3 месяцев базисные препараты должны быть заменены или использованы их комбинации с ГКС в малых дозах, что позволяет снизить активность ревматоидного артрита до начала действия первых. Шесть месяцев — критический срок, не позднее которого должна быть подобрана действенная базисная терапия.
Лучшим препаратом для начала базисной терапии при тяжёлом течении ревматоидного артрита и РФ-позитивности, наличии внесуставных проявлений считается метотрексат — цитостатический иммунодепрессант, который хорошо переносится при длительном применении и имеет меньше побочных эффектов, чем другие лекарственные средства данной группы.
Новым подходом является использование высоких доз ГКС (пульс-терапия) в комбинации с медленно действующими средствами, что позволяет повысить эффективность последних; комбинаций метотрексата с аминохинолиновыми производными, солями золота, сульфазалазином, а также селективным иммунодепрессантом циклоспорином А.
При высокой степени активности воспалительного процесса используют ГКС, причём в случаях системных проявлений ревматоидного артрита — в виде пульс-терапии (только ГКС или в сочетании с цитостатиком — циклофосфамидом), без системных проявлений — в виде курсового лечения. ГКС также применяют как поддерживающую противовоспалительную терапию при неэффективности других лекарственных средств.
В ряде случаев ГКС используются в качестве локальной терапии. Показаниями к их применению являются: преимущественно моно- или олигоартрит крупных суставов; затянувшийся экссудативный процесс в суставе; преобладание «локального статуса» над системным; наличие противопоказаний к системному использованию ГКС. При внутрисуставном введении депо-формы кортикостероидов оказывают и системное действие. Препаратом выбора является Дипроспан, оказывающий пролонгированное действие.
При ревматоидном артрите синовиальные мембраны, по невыясненным причинам, секретируют большое количество фермента глюкозо-6-фосфат дегидрогеназы которая также разрушает дисульфидные связи в клеточной мембране. При этом наблюдается «утечка» протеолитических ферментов из клеточных лизосом, которые вызывают повреждения близлежащих костей и хрящей. Организм отвечает на это путём выработки цитокинов, среди которых также есть фактор некроза опухоли α TNF-α. Каскады реакций в клетках, которые запускаются цитокинами, ещё больше усугубляют симптомы болезни. Хроническое ревматоидное воспаление, ассоциированное с TNF-α, очень часто вызывает повреждения хрящей и суставов, ведущие к физической нетрудоспособности.
В лечении используются моноклональное антитело к цитокину TNF-α, которое эффективно с высокой афинностью (до 10X10 −1 М) связывается с TNF в его как растворимой, так и трансмембранной формах, результируя нейтрализацию активности TNF.
Дата добавления: 2015-06-15 ; просмотров: 1688 . Нарушение авторских прав
Ревматоидный артрит. Этиология и патогенез
Ревматоидный артрит — хроническое системное аутоиммунное заболевание соединительной ткани, сопровождающееся преимущественным поражением периферических суставов с развитием в них эрозивно-деструктивных изменений и анкилозирования.
На долю РА приходится 10% от общего числа ревматических болезней, а ежегодная частота возникновения новых случаев заболевания составляет около 0,02%. Ревматоидный артрит (РА) — одно из наиболее распространенных хронических воспалительных заболеваний человека, частота которого в популяции, согласно данным ВОЗ, составляет от 0,6 до 1,3%, а у близких родственников она достигает 3—5%. Женщины болеют значительно чаще по сравнению с мужчинами (соотношение 3:1). Основными симптомами РА являются постоянные боли в суставах воспалительного характера и прогрессирующее нарушение их функций, что приводит к снижению качества жизни пациентов и ранней инвалидности. Так, почти 50% больных РА становятся инвалидами в течение 5 лет заболевания, а 10% — в течение первых двух лет болезни.
Продолжительность жизни при РА, согласно данным проспективных исследований, также уменьшается из-за сопутствующих заболеваний (инфекции, поражение сердечно-сосудистой системы, почек, легких и др.), развитие которых связывается как с прогрессированием иммуновоспалительного процесса, так и с ятрогенной иммуносупрессией.
Этиология и патогенез
До настоящего времени этиология РА остается неизвестной. Возможно, в развитии заболевания определенную триггерную роль играют некоторые вирусы — вирус Эпштейна—Барр, лимфотропный Т-клеточный вирус, человеческий парвовирус В19 и др. В частности, антитела к вирусу Эпштейна—Барр (ВЭБ) в высоких титрах выявляются у 80% больных РА; выявлена более высокая частота инфицирования ВЭБ лимфоцитов у пациентов с РА по сравнению с клетками здоровых доноров. В эксперименте развитие артрита у мышей вызывалось культурой ретровирусов, выделенных из синовиальной жидкости больных РА. Рассматривается точка зрения о том, что вирусная инфекция может запускать процесс поликлональной В-клеточной активации с последующим синтезом ревматоидных факторов плазмоцитами, что и наблюдается при РА.
Развитие РА также связывается с генетической предрасположенностью, которая ассоциируется со вторым классом генов главного комплекса гистосовместимости HLA. Так, около 90% больных являются носителями HLA-DR1 или одного из трех вариантов локуса HLA-DR4 (Dw4, Dwl4 или Dwl5). При этом носительство HLA-DR4 у больных с серопозитивным РА достигает 70%, в то время как в популяции частота его встречаемости не превышает 25%. Влияние этих антигенов системы HLA на развитие РА связывается с наличием в них общих аминокислотных последовательностей (глутамин-лизин), определяющих предрасположенность к заболеванию. Кроме того, имеется определенная связь между локусом HLA-DR4 и тяжестью течения РА, а также гиперпродукцией ревматоидных факторов и быстрым развитием эрозивных изменений в суставах.
Инициальные воспалительные изменения происходят в синовиальной оболочке суставов, куда «рекрутируются» иммунокомпетентные клетки, продуцирующие провоспалительные цитокины, а также антитела к компонентам синовии. Увеличение в полости сустава концентрации веществ с потенциально аутоантигенными свойствами еще больше усиливает иммуновоспалительную реакцию, вызывающую дальнейшее повреждение суставных тканей. При этом активация и агрессивная пролиферация синовиальных клеток, а также суставных макрофагов модулируется различными колониестимулирующими факторами (КСФ-ГМ, КСФ-Г), цитокинами, продуктами метаболизма арахидоновой кислоты и другими медиаторными субстанциями.
В частности, антиген-специфическая активация С04+Т-лимфоцитов по ТЫ типу, характерная для РА, приводит к гиперпродукции интерлейкина (ИЛ)-2, интерферона-у, ИЛ-17, а также к дисбалансу между провоспалительными (фактор некроза опухоли а — ФНО-а, ИЛ-1в, ИЛ-6, ИЛ-8 и др.) и антивоспалительными цитокинами (ИЛ-4, ИЛ-10, растворимый антагонист ИЛ-1в и др.) с преобладанием продукции первых над вторыми.
Не исключено, что запуск Т-клеточного звена иммунитета может происходить под действием у-интерферона (ИФН-у), продукция которого увеличивается в ответ на вирусную инфекцию. В свою очередь, активированные Т-хелперы I типа, продуцируя ИЛ-2 и целый ряд провоспалительных цитокинов, индуцируют пролиферацию В-лимфоцитов и, соответственно, продукцию антител. Наконец, под влиянием того или иного биологического агента происходит значительное повышение содержания С3b и компонентов комплемента, что может вести, в свою очередь, к стимуляции Т-лимфоцитов I типа, а увеличение продукции макрофагами трансформирующего фактора роста в (TGF-p) способствует активации Т-хелперов III типа, причем этот процесс протекает без наличия антигена.
Таким образом, под влиянием пока не установленного этиологического фактора и наличии предрасполагающих факторов в патологический процесс могут вовлекаться практически все компоненты иммунной системы, однако ведущее патогенетическое значение в развитии РА придается нарушениям в ее Т- и В-клеточных звеньях.
Фактору некроза опухолей а придается особое значение в иммунопатогенезе РА. Считается, что в дебюте заболевания преобладает синтез именно этого цитокина, который обладает способностью запускать целый каскад иммунопатологических реакций, в том числе стимулировать продукцию других провоспалительных субстанций, а неконтролируемый синтез ФНО-а лежит в основе хронизации патологического процесса и прогрессирующих костных деструктивных изменений. В частности, ФНО-а принимает участие в развитии клинических признаков воспаления (боль, лихорадка, снижение массы тела и др.), индуцирует экспрессию молекул адгезии, стимулирует неоангиогенез, пролиферацию фибробластов, играющих важную роль в формировании ревматоидного паннуса и т.д.
В результате возникших иммунных нарушений В-лимфоциты продуцируют агрегированный IgG, обладающий способностью вступать в иммунную реакцию по типу антиген — антитело. Воспринимая измененный IgG как чужеродный антиген, плазматические клетки синовиальной оболочки вырабатывают антитела — ревматоидные факторы (РФ) — классов IgG и IgM. Результатом взаимодействия макрофагов, Т- и В-лимфоцитов является выработка антител, образующих при соединении с антигеном иммунные комплексы, которые циркулируют в периферической крови и откладываются в тканях, вызывая их повреждение (рис. 4.1). В недавних исследованиях было убедительно показано, что не только РФ, но и аутоантитела с другой специфичностью (например, антикератиновые антитела, антиперинуклеарный фактор и др.) могут играть важную роль в развитии заболевания.
Таким образом, в основе патогенеза РА лежат глубокие нарушения иммунного ответа с дисбалансом количественного и качественного состава иммунокомпетентных клеток, с нарушением их функциональной активности и клеточной кооперации. При этом максимальные воспалительные изменения, индуцируемые резидентными синовиальными клетками (синовиоцитами А, фибробластами, дендритными клетками, Т- и В-лимфоцитами), в дебюте заболевания наблюдаются именно в синовиальной оболочке суставов, приводя к ее гиперплазии и быстрому увеличению объема синовиальной ткани (паннус), разрушающей суставной хрящ и подлежащую субхондральную кость. При прогрессировании иммунных нарушений формируется типичная клиническая картина РА с вовлечением в патологический процесс многих органов и систем организма.