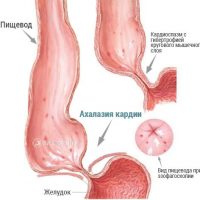
Ахалазия кардии
Главная угроза ахалазии – критическое увеличение размеров пищевода, приводящее к полной потере функции глотания. В этом случае пациенту требуется сложная и травматичная операция – экстирпация (удаление) пищевода и создание нового пищевода из части желудка.
- Что такое ахалазия кардии
Нижний пищеводный сфинктер (кардиальный сфинктер) располагается в месте перехода пищевода в желудок. При нормальном акте глотания пища перемещается вниз по пищеводу и подходит к области нижнего пищеводного сфинктера, его мышечные волокна рефлекторно расслабляются, и пища попадает в желудок. При ахалазии мышечные циркулярные волокна, из которых состоит нижний пищеводный сфинктер, пропускающий пищу в желудок, не расслабляются или расслабляются с трудом. Пища не имеет возможности свободно поступать в желудок. Она скапливается в пищеводе, вызывая его тракционное расширение.
Основная причина возникновения ахалазии – психоэмоциональный фактор. Эмоциональная среда в крупных городах неблагоприятна, пациенты испытывают стресс на работе и дома, поэтому в наше время ахалазия – довольно распространённое заболевание. Если пациент приходит на консультацию и говорит: «Доктор, я сильно понервничал, и после этого начало ломить за грудиной. Я плохо глотаю пищу, как комок в горле стоит…» – в первую очередь врач предполагает ахалазию. Если с вами происходит нечто похожее – не тяните с визитом к врачу. Чем дольше у пациента существует ахалазия, тем более выраженными становятся клинические проявления ахалазии.
Главным симптомом ахалазии является дисфагия – нарушение глотания. На начальных стадиях ахалазии жидкость проглатывается хуже, чем твёрдая пища. Если в пищевод попадает твёрдая пища, то перистальтика пищевода проталкивает её в желудок через напряженный кардиальный сфинктер. На жидкость перистальтика пищевода практически не влияет. Жидкость задерживается в пищеводе и проглатывается хуже. Ещё один важный симптомом ахалазии – боль в конце акта глотания. Пища проходит по пищеводу до нижнего сфинктера. Перистальтические движения пищевода пытаются протолкнуть её через сжатый сфинктер, в результате возникает достаточно интенсивная боль.
Кроме дисфагии и боли, существуют внепищеводные проявления ахалазии – аспирационные бронхиты и аспирационные пневмонии. Если пища не прошла в желудок – она осталась в пищеводе. Пациент принимает горизонтальное положение и засыпает – содержимое пищевода вытекает в ротовую полость и проникает в бронхи и лёгкие во время вдоха (аспирация). В результате развиваются аспирационные бронхиты и пневмонии. Кроме того, при аспирации пищи существует риск рефлекторной остановки дыхания.
Повышенное давление в пищеводе может приводить к развитию дивертикулов, которые со временем увеличиваются в размерах. Дивертикулам пищевода посвящена отдельная статья. Но чаще у пациента с ахалазией возникает расширение просвета пищевода. И чем дольше существует ахалазия, тем больше в диаметре его пищевод. На поздней стадии ахалазии расширение пищевода становится необратимым.

Источник изображения: Timonina/Shutterstock
Для диагностики и определения стадии ахалазии в Ильинской больнице применяются рентгенологическое исследование с водорастворимым контрастном (в некоторых случаях КТ с контрастом) и эндоскопическое исследование. Различают 4 стадии ахалазии. Чем больше расширение пищевода, тем выше стадия ахалазии. На 1 и 2 стадиях просвет пищевода увеличен. На 3 и 4 стадиях пищевод меняет свою анатомическую конфигурацию, стремясь к S-образной форме. На 4 стадии размер пищевода может превысить размер желудка.
- Малотравматичная эндоскопическая операция
Пациентам с 1, 2 и 3 стадиями ахалазии хирурги Ильинской больницы выполняют малоинвазивную эндоскопическую операцию – пероральную эзофагокардиомиотомию – POEM (peroral esophageal myotomy). Операция проводится без внешних разрезов. Специальный тонкий эндоскоп вводится в пищевод, через инструментальный канал эндоскопа проводятся микроминиатюрные хирургические инструменты. Отступив порядка 10 см от нижнего пищеводного сфинктера, хирург отслаивает слизистую оболочку пищевода от мышечного слоя, создавая «туннель». Эндоскоп вводится в подслизистый слой и постепенно продвигается в сторону сфинктера. Задача эндоскопического хирурга – рассечь мышечные волокна пищевода в зоне около 7 см от сфинктера, дойти до циркулярных мышечных волокон сфинктера и полностью их пересечь. После рассечения мышечных волокон эндоскоп извлекается, место доступа закрывается с помощью специальных клипс, операция завершается. Проведение пероральной эзофагокардиомиотомии возможно на 1, 2 и 3 стадии ахалазии. Однако есть научные данные, говорящие о том, что и при 4 стадии эта операция дает хороший эффект.
- Лапароскопическая операция
3 стадия ахалазии не всегда позволяет выполнить эндоскопическую операцию. В этом случае хирурги Ильинской больницы проводят лапароскопическую эзофагокардиомиотомию, так называемую операцию Геллера. На передней брюшной стенке производятся пять небольших разреза, через которые в брюшную полость проводятся лапароскоп и хирургические манипуляторы. Хирург проходит к области нижнего пищевого сфинктера и очень точно пересекает его циркулярные мышечные волокна. Затем производится фундопликация по Дору – часть желудка заворачивается вокруг пищеводно-желудочного перехода и берет на себя функцию сфинктера, что позволяет избежать развития гастро-эзофагиального рефлюкса (заброса кислоты из желудка в пищевод).
У пациентов с 4 стадией ахалазии пищевод S-образно изменён и максимально расширен, его просвет может превышать 10 см. Перистальтика такого пищевода либо неэффективна, либо её вообще нет – пищевод не выполняет свою функцию. Таким пациентам может помочь только экстирпация пищевода – операция по полному удалению пищевода. Неработающий пищевод практически полностью удаляется. Часть стенки желудка забирается и из нее формируется новый пищевод. Операция длится около 10 часов.
В Ильинской больнице реализована концепция хирургии ускоренной реабилитации (fast track хирургия). Эта идеология основана на результатах многолетних международных клинических исследований, признана и внедрена во всех развитых странах. Она включает в себя упрощенную подготовку к операции, выполнение операции в день госпитализации, минимизацию хирургического доступа (лапароскопия и эндоскопия), максимальные усилия по сохранению пораженного органа (вместо удаления органа), раннее пробуждение пациента после наркоза, раннюю мобилизацию пациента (можно вставать на ноги вскоре после операции), раннюю алиментацию (можно начинать есть и пить вскоре после операции). Этот комплекс мер направлен на максимально быструю реабилитацию пациента после хирургического вмешательства и восстановление качества его жизни.
Пациенты Ильинской больницы не испытывают боли – за этим следит специальный общегоспитальный сервис – Служба лечения боли. В арсенале наших специалистов полный спектр анальгетиков, включая мощные опиодные препараты, и высокотехнологичные инструментальные методики, которые хорошо себя зарекомендовали на западе, но редко применяются в нашей стране.
Для наиболее тяжелых пациентов, прошедших лечение в условиях нашего стационара, мы готовы организовать «стационар на дому». Даже после проведения самой сложной и тяжелой хирургической операции, больной может быть переведен домой достаточно быстро. Домашняя среда и близость семьи способствуют скорейшему выздоровлению. Мы обеспечиваем постоянное наблюдение за пациентом с помощью специально подобранного набора мониторов, контролируем лекарственную терапию и организуем регулярные занятия с инструктором-реабилитологом. В домашних условиях с успехом могут проводиться внутривенные вливания, масочная вентиляция легких и другие процедуры и манипуляции.
Евсютина Ю.В., Сторонова О.А., Трухманов А.С., Ивашкин В.Т. Ахалазия кардии: современные представления об этиологии, патогенезе, клинической картине и диагностике // РЖГГК. 2014. № 6. С. 4–12.
Цель обзора. Представить современные данные об этиологии, патогенезе, клинической картине и диагностике ахалазии кардии.
Основные положения. Ахалазия кардии представляет собой первичное двигательное заболевание пищевода, при котором происходит поражение межмышечных сплетений.
Основными симптомами ахалазии являются: дисфагия, регургитация, боль в грудной клетке и похудание. «Золотым стандартом» диагностики является манометрия пищевода, которая позволяет оценить давление покоя и расслабления нижнего пищеводного сфинктера и перистальтическую активность дистального отдела пищевода.
В качестве возможных этиологических факторов рассматриваются генетическая, аутоиммунная и инфекционная теории.
Заключение. На настоящий момент патогенез, клиническая картина и методы диагностики ахалазии кардии изучены достаточно подробно, однако этиология заболевания, несмотря на многовековую историю вопроса, остается неизвестной. Большого внимания заслуживает аутоиммунная теория заболевания, которая требует проведения дальнейших исследований.
Ключевые слова: ахалазия кардии, аутоантитела, дисфагия.
Евсютина Юлия Викторовна — клинический ординатор кафедры пропедевтики внутренних болезней ГБОУ ВПО «Первый МГМУ им. И. М. Сеченова». Контактная информация: uselina@mail.ru, 119991, Москва, ул. Погодинская, д. 1, стр. 1. Клиника пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В. Х. Василенко ГБОУ ВПО «Первый МГМУ им. И. М. Сеченова»
Трухманов Александр Сергеевич — доктор медицинских наук, профессор кафедры пропедевтики внутренних болезней ГБОУ ВПО «Первый МГМУ им. И. М. Сеченова»
Cardiac achalasia: modern concepts on etiology, pathogenesis, clinical presentation and diagnostics
Yu. V. Yevsyutina, O. A. Storonova, A. S. Trukhmanov, V. T. Ivashkin
Chair of internal diseases propedeutics, medical faculty, State educational government-financed institution of higher professional education «Sechenov First Moscow state medical university» Ministry of Healthcare of the Russian Federation
The aim of review. To present up-to-date data on etiology, pathogenesis, clinical presentation and diagnostics of cardiac achalasia.
Key points. Cardiac achalasia represents primary esophageal motor disease with involvement of myenteric plexus.
Basic symptoms of achalasia include dysphagia, regurgitation, chest pain and weight loss. Esophageal manometry which allows to evaluate resting pressure and relaxation phenomenon of the lower esophageal sphincter and peristaltic activity of distal part of the esophagus is the «gold standard» of diagnostics.
Genetic, autoimmune and infectious theories are considered for disease etiology.
Conclusion. For the present moment pathogenesis, clinical presentation and diagnostics methods of cardiac achalasia are investigated in detail, however etiology of disease remains unknown, despite of centuries-old history. The major attention is drawn to autoimmune theory which requires further investigations.
Key words: cardiac achalasia, autoantibodies, dysphagia.
Yevsyutina Yuliya V — attending physician, Chair of internal diseases propedeutics, medical faculty, State educational government-financed institution of higher professional education «Sechenov First Moscow state medical university».
Contact information: uselina@mail.ru; 119991, Moscow, Pogodinskaya street, 1, bld 1. Vasilenko Clinic of internal diseases propedeutics, gastroenterology and hepatology State educational government-financed institution of higher professional education «Sechenov First Moscow state medical university»
Trukhmanov Aleksander S — MD, PhD, professor, Chair of internal diseases propedeutics, medical faculty, State educational government-financed institution of higher professional education «Sechenov First Moscow state medical university»
Ахалазия кардии представляет собой идиопатическое заболевание, причиной развития которого является воспаление и дегенерация межмышечных сплетений, приводящие к потере постганглионарных тормозящих нейронов, необходимых для расслабления нижнего пищеводного сфинктера (НПС) и перистальтических сокращений пищевода [33].
Очень часто кардиоспазм считают синонимом ахалазии кардии наряду с мегаэзофагусом и идиопатическим расширением пищевода, однако это утверждение является ошибочным. Кардиоспазм представляет собой заболевание, характеризующееся стойким спазмом кардии, возникающим в результате дегенеративно-дистрофических изменений преганглионарных нейронов дорсальных ядер блуждающих нервов [10]. В пользу различия этих заболеваний говорит и тот факт, что баллонная пневмокардиадилатация как метод лечения эффективен только при ахалазии кардии.
Первый случай ахалазии кардии был описан в 1674 г. английским доктором T. Williams, который успешно вылечил пациента с постоянной прогрессирующей рвотой расширением пищевода с помощью китового уса [49]. Спустя 250 лет, в 1927 г., A. Hurst, наблюдавший около 20 пациентов с дисфагией и рвотой, предположил, что их причиной может быть отсутствие нормального расслабления НПС вследствие органического поражения ауэрбахова нервного сплетения, и впервые ввел термин «ахалазия», определив ее как отсутствие релаксации (от греч, а — отсутствие, chalasis — расслабление) [21]. Но несмотря на многовековую историю изучения этого заболевания, его этиология по сей день остается неизвестной для исследователей.
Перистальтика пищевода и расслабление НПС контролируются энтеральной нервной системой (ЭНС), представляющей собой сложную сеть нервов и сплетений, работу которых координируют ЦНС и ядра блуждающего нерва, расположенные в дне IV желудочка. Нейроны, входящие в состав ЭНС, контролируют двигательную активность желудочно-кишечного тракта (ЖКТ) и располагаются в ауэрбаховом межмышечном нервном сплетении. Существуют два основных типа нейронов:1) тормозящие, нейротрансмиттерами которых являются оксид азота (NO) и вазоактивный интестиналъный пептид (ВИП), и 2) возбуждающие, медиатором которых является ацетилхолин (АХ) [18].
Гистологическое исследование материала, взятого при аутопсии и миотомии, показывает, что в межмышечных сплетениях развивается воспаление, в котором принимают участие CD3/ CD8-позитивные цитотоксические Т-лимфоциты, эозинофилы, тучные клетки, происходит потеря ганглионарных клеток и развивается фиброз [48]. На начальных стадиях заболевания преобладает воспалительный компонент с поражением главным образом тормозящих нейронов, в которых осуществляется синтез NO и ВИП. При дальнейшем прогрессировании заболевания отмечаются полная потеря этих клеток и замещение их соединительной тканью [19]. Потеря тормозящих нейронов приводит к неполному расслаблению НПС. А характерное для ахалазии отсутствие перистальтики пищевода развивается в связи с потерей нейронов, нейротрансмиттером которых является NO [23].
Ахалазия кардии считается достаточно редким заболеванием, ее распространенность составляет 10 случаев на 100 000 населения [23]. Идиопатическая ахалазия встречается на всех континентах, причем мужчины и женщины подвержены этому заболеванию одинаково [38]. У взрослых ахалазию кардии чаще всего диагностируют в возрастной группе от 25 до 60 лет. На настоящий момент рассматриваются три основные этиологические гипотезы: генетическая, инфекционная и аутоиммунная.
Генетическая гипотеза
У детей самой частой причиной ахалазии кардии является мутация гена ALADIN 12q13, что приводит к развитию аутосомнорецессивного заболевания, так называемого синдрома Allgrove, или синдрома ААА, характеризующегося развитием ахалазии, алакримии и болезни Аддисона [41].
Риск развития ахалазии повышен и у детей с трисомией 21 (болезнью Дауна). Примерно 75% таких пациентов имеют заболевания ЖКТ и у 2% развивается ахалазия [28]. Риск ахалазии у детей с синдромом Дауна выше в 200 раз, чем в обшей популяции [50].
Еще одна теория, указывающая на роль генетических факторов в развитии ахалазии, связана с полиморфизмом гена IL23R, локализованного в хромосоме Ip31 Она находит свое подтверждение в исследовании, проведенном в Испании, в ходе которого изучался полиморфизм гена IL23R Arg381 Gln у 262 пациентов с ахалазией и 802 здоровых людей. Установлено, что у мужчин младше 40 лет с ахалазией достоверно чаще встречается полиморфизм данного гена, что позволяет сделать вывод о важной роли IL23R как предрасполагающего фактора в развитии идиопатической ахалазии кардии [13].
Найдена также ассоциация между ахалазией кардии и специфическим HLA-генотипом. Исследование, проведенное в 2002 г., изучавшее уровень циркулирующих аутоантител с HLA DQA1- и DQB1-аллелями у пациентов с ахалазией и здоровых лиц, показало, что у всех женщин и 66,7% мужчин с идиопатической ахалазией и DQA1 * 0103 и DQB1 * 0603-аллелями выявлены аутоантитела к межмышечным сплетениям [35].
Заслуживает внимания теория о полиморфизме NO-синтазы (NOS), которая представляет собой фермент, катализирующий образование NO из аргинина, кислорода и NADPH. Существуют три типа NOS: нейрональная (nNOS), индуцибельная (iNOS) и эндотелиальная (eNOS). Ответственные за них гены локализуются в хромосомах:12q24.2, 17q11.2 q12 и 7q36. В ряде работ показан полиморфизм всех трех генов у пациентов с ахалазией. При этом чаще всего выявлялся полиморфизм iNOS22*A/Ab и eNOS*4a4a [27, 47].
Кроме оксида азота, вторым нейротрансмиттером тормозящих нейронов является вазоактивный интестинальный пептид. Одним из его рецепторов является рецептор 1, который принадлежит к семейству секретиновых и экспрессируется различными иммунными клетками, такими как Т-лимфоциты, макрофаги и дендритные клетки [32]. Полиморфизм этого гена (VIPR1) также может играть роль в развитии идиопатической аха-лазии. VIPR1-ген локализуется в хромосоме 3p22, и в ходе некоторых исследований были показаны пять его простых нуклеотидных полиморфизма, таких как (rs421558) Intron-1, (rs437876) Intron-4, (rs417387) Intron-6, rs896 и rs9677 (3’UTR) [31, 32].
Ген, ответственный за синтез протеинтирозинфосфатазы нерецепторного типа 22 (PTPN22), локализуется в хромосоме 1p13.м3-p13 и ассоциирован с развитием аутоиммунных заболеваний [13]. Одной из кодируемой им фосфатаз является специфическая лимфоидная фосфатаза (Lyp), которая представляет собой внутриклеточную тирозиновую фосфатазу, являющуюся важнейшим регулятором Т-клеточной активации [22]. Полиморфизм гена PTPN22 С1858T, когда происходит замена кодона 620 Arg (R) на Trp (W), вследствие чего вместо Lyp-R620 образуется Lyp-W620 и повышается активность Т-лимфоцитов, является фактором риска развития аутоиммунных заболеваний [42, 44]. Исследование, проведенное в Испании, показало, что вышеописанный полиморфизм повышает риск ахалазии в испанской популяции [36].
Инфекционная гипотеза
В течение многих лет болезнь Чагаса рассматривают как один из этиологических факторов в развитии ахалазии кардии. Это заболевание, называемое также американским трипаносомозом, вызывается микроорганизмом Trypanosoma cruzi и встречается в странах Латинской Америки. Заболевание протекает в две фазы. Первая является острой и связана с циркуляцией паразитов в крови. Вторая фаза проявляется в проникновении трипаносом в сердце и мышечный слой пищевода, где и происходит их кумуляция. Процесс сопровождается в основном поражением межмышечных сплетений пищевода, что приводит к последующим дегенеративным изменениям в них и нарушению двигательной функции пищевода. Именно в эту фазу происходит нарушение расслабления НПС и развивается атония пищевода, которые проявляются дисфагией, пищеводной рвотой и болью по ходу пищевода при проглатывании пищи [11].
В качестве возможного этиологического фактора идиопатической ахалазии высказывается также предположение о вирусной природе заболевания. Так, существует некая корреляция между ахалазией кардии и предшествующими инфекционными заболеваниями, в частности корью и опоясывающим лишаем, возбудителем которого является Herpes zoster [30].
Аутоиммунная теория
Аутоиммунная теория в патогенезе ахалазии заслуживает отдельного внимания. Интересен тот факт, что одинаковые аутоантитела могут встречаться как при паранеопластических, так и идиопатических нарушениях моторики ЖКТ [24]. Примерами могут служить частое обнаружение антинейрональных нуклеарных антител (ANNA-1) при мелкоклеточном раке легких и антител к клеткам Пуркинье (PCA-1) при карциноме яичников и молочных желез, при сопутствующих им нарушениях двигательной функции пищевода [25, 29].
Как установлено в ряде работ, в популяции пациентов с ахалазией кардии возрастает риск развития аутоиммунных заболеваний. Так, проведенное в Канаде исследование, включавшее 193 пациента с диагнозом идиопатичекой ахалазии, показало повышенный риск развития некоторых аутоиммунных заболеваний у этих пациентов в сравнении с контрольной группой: сахарного диабета 1-го типа в 5,4 раза, гипотиреоза в 8,5 раза, синдрома Шегрена в 37 раз, системной красной волчанки в 43 раза и увеита в 259 раз, что в общем дает повышение риска аутоиммунных заболеваний у пациентов с ахалазией в 3,6 раза [12].
В некоторых исследованиях доказано сочетание ахалазии кардии и тиреоидной патологии. Так, в исследовании, проведенном в Иране в 2007 г., среди 30 пациентов с ахалазией у 23,2% выявлена патология щитовидной железы, из них у 13,3% — гипотиреоз, у 6,6% — гипертиреоз и у 3,3% — эутиреоидный зоб [15].
В одном из последних исследований, выполненном в клинике Мэйо в США, изучался профиль циркулирующих аутоантител у больных с первичной ахалазией (n=70) и здоровых людей (n=161) [34]. Пациенты с ахалазией подвергались тщательному сбору анамнеза: уточнялись данные о наличии сахарного диабета 1-го типа, тиреоидной патологии, пернициозной анемии, витилиго, ревматоидного артрита, системной красной волчанки, табакокурении, влиянии профессиональных вредностей, а также отягощенном семейном анамнезе по ахалазии, онкологическим и аутоиммунным заболеваниям. У всех пациентов исследовалась сыворотка крови на спектр нейрональных аутоантител: антитела к никотиновым рецепторам АХ — ганглионарному и мышечному типу (AChR), антитела к калиевым и кальциевым каналам — P/Q-тип и N-тип, к декарбоксилазе глутаминовой кислоты (GAD65), антитела к скелетным мышцам, антинейрональные нуклеарные антитела (ANNA-1), известные также под названием anti-Hu, и другие органоспецифичные антитела: маркёры сахарного диабета 1-го типа — антитела к инсулину, к клеткам островков Лангерганса, антитела к париетальным клеткам желудка и тиреопероксидазе.
Согласно результатам, представленным в табл. 1, ни у пациентов с ахалазией, ни в контрольной группе не было обнаружено антинуклеарных нейрональных антител и антител к ганглионарным рецепторам АХ, которые могут иметь место при паранеопластической ахалазии. Однако 25,7% больных с первичной ахалазией имели одно или более нейрональных антител к скелетной мускулатуре, тогда как в контрольной группе они были выявлены лишь у 4,4%. Среди пациентов с ахалазией у 21,4% найдены антитела к декарбоксилазе глутаминовой кислоты (в контрольной группе у 2,5%), хотя только один пациент страдал сахарным диабетом 1-го типа. Данное исследование, как и вышеупомянутые, показало также, что у больных с первичной ахалазией достоверно выше уровень органоспецифических антител: к тиреопероксидазе (выявлены в 20% в группе ахалазии по сравнению с 12,4% в контрольной группе) и антител к париетальным клеткам желудка — 5,7% против 1,9%.
Ахалазия кардии
Ахалазия кардии – это отсутствие расслабления или недостаточное расслабление нижнего отдела пищевода нейрогенной этиологии. Сопровождается расстройством рефлекторного открытия кардиального отверстия во время акта глотания и нарушением попадания пищевых масс из пищевода в желудок. Ахалазия кардии проявляется дисфагией, регургитацией и болями в эпигастрии. Ведущими методами диагностики служат рентгеноскопия пищевода, эзофагоскопия, эзофагоманометрия. Консервативное лечение заключается в проведении пневмокардиодилатации; хирургическое – в выполнении кардиомиотомии.
МКБ-10
Общие сведения
Ахалазия кардии в медицинской литературе иногда обозначается терминами мегаэзофагус, кардиоспазм, идиопатическое расширение пищевода. Ахалазия кардии, по разным данным, в практической гастроэнтерологии составляет от 3 до 20% всех заболеваний пищевода. Среди причин, вызывающих нарушение проходимости пищевода, кардиоспазм стоит на третьем месте после рака пищевода и послеожоговых рубцовых стриктур.
Патология с одинаковой частотой поражает женщин и мужчин, чаще развивается в возрасте 20-40 лет. При ахалазии кардии в результате нервно-мышечных нарушений снижается перистальтика и тонус пищевода, не происходит рефлекторного расслабления пищеводного сфинктера при глотании, что затрудняет эвакуацию пищи из пищевода в желудок.

Причины
Выдвинуто множество этиологических теорий происхождения ахалазии кардии, которые связывают развитие патологии с врожденным дефектом нервных сплетений пищевода, вторичным повреждением нервных волокон при туберкулезном бронхоадените, инфекционных или вирусных заболеваниях; дефицитом витамина В и т. д. Распространена концепция нарушений центральной регуляции функций пищевода, рассматривающая ахалазию кардии как следствие нервно-психических травм, ведущих к расстройству корковой нейродинамики, иннервации пищевода, дискоординации в работе кардиального сфинктера. Однако до конца факторы, способствующие развитию заболевания, остаются невыясненными.
Ведущая роль в патогенезе ахалазии кардии отводится поражению отделов парасимпатической нервной системы, регулирующей моторику пищевода и желудка (в частности ауэрбаховского сплетения). Вторичная (симптоматическая) ахалазия кардии может быть вызвана инфильтрацией сплетения злокачественной опухолью (аденокарциномой желудка, гепатоцеллюлярным раком, лимфогранулематозом, раком легкого и др.). В ряде случаев ауэрбаховское сплетение может поражаться при миастении, гипотиреозе, полиомиозите, системной красной волчанке.
Патогенез
Фактическая денервация верхних отделов ЖКТ вызывает снижение перистальтики и тонуса пищевода, невозможность физиологического расслабления кардиального отверстия во время акта глотания, мышечную атонию. При таких нарушениях пища поступает в желудок только благодаря механическому раскрытию кардиального отверстия, происходящего под гидростатическим давлением жидких пищевых масс, скопившихся в пищеводе. Длительный застой пищевого комка приводит к расширению пищевода – мегаэзофагусу.
Морфологические изменения в стенке пищевода зависят от длительности существования ахалазии кардии. В стадии клинических проявлений отмечается сужение кардии и расширение просвета пищевода, его удлинение и S-образная деформация, огрубление слизистой оболочки и сглаживание складчатости пищевода. Микроскопические изменения при ахалазии кардии представлены гипертрофией гладкомышечных волокон, разрастанием в пищеводной стенке соединительной ткани, выраженными изменениями в межмышечных нервных сплетениях.
Классификация
По выраженности нарушений функций пищевода выделяют стадии компенсации, декомпенсации и резкой декомпенсации ахалазии кардии. Среди множества предложенных вариантов классификации наибольший клинический интерес представляет следующий вариант стадирования:
- I стадия. Характеризуется интермиттирующим спазмом кардиального отдела. Макроскопических изменений (стеноза кардии и супрастенотического расширения просвета пищевода) не отмечается.
- II стадия. Спазм кардии носит стабильный характер, наблюдается незначительное расширение пищевода.
- III стадия. Выявляется рубцовая деформация мышечного слоя кардии и резкое супрастенотическое расширение пищевода.
- IV стадия. Протекает с резко выраженным стенозом кардиального отдела и значительной дилатацией пищевода. Характеризуется явлениями эзофагита с изъязвлением и некрозами слизистой, периэзофагитом, фиброзным медиастинитом.
В соответствии с рентгенологическими признаками различают два типа ахалазии кардии. Первый тип патологии характеризуется умеренным сужением дистального отрезка пищевода, одновременной гипертрофией и дистрофией его циркулярных мышц. Дилатация пищевода выражена умеренно, участок расширения имеет цилиндрическую или овальную формы. Ахалазия кардии первого типа встречается у 59,2% пациентов.
О втором типе ахалазии кардии говорят при значительном сужении дистального участка пищевода, атрофии его мышечной оболочки и частичном замещении мышечных волокон соединительной тканью. Отмечается выраженное (до 16-18 см) расширение супрастенотического отдела пищевода и его S-образная деформация. Ахалазия кардии первого типа со временем может прогрессировать во второй тип. Знание типа ахалазии кардии позволяет гастроэнтерологам предусмотреть возможные трудности при проведении пневмокардиодилатации.
Симптомы ахалазии кардии
Клиническими проявлениями патологии служат дисфагия, регургитация и загрудинные боли. Дисфагия характеризуется затруднением глотания пищи. В некоторых случаях нарушение акта глотания развивается одномоментно и протекает стабильно; обычно дисфагии предшествует грипп или другое вирусное заболевание, стресс. У части пациентов дисфагия вначале носит эпизодический характер (например, при торопливой еде), затем становится более регулярной, затрудняющей прохождение как плотной, так и жидкой пищи.
Дисфагия при ахалазии кардии может быть избирательной и возникать при употреблении только определенного вида пищи. Приспосабливаясь к нарушению глотания, пациенты могут самостоятельно находить способы регуляции прохождения пищевых масс – задерживать дыхание, заглатывать воздух, запивать пищу водой и т. д. Иногда при ахалазии кардии развивается парадоксальная дисфагия, при которой прохождение жидкой пищи затрудняется в большей степени, чем твердой.
Регургитация при ахалазии кардии развивается в результате обратного заброса пищевых масс в полость рта при сокращении мышц пищевода. Выраженность регургитации может носить характер небольшого срыгивания или пищеводной рвоты, когда развивается обильное срыгивание «полным ртом». Регургитация может быть периодической (например, в процессе еды, одновременно с дисфагией), возникать сразу после приема пищи или спустя 2-3 часа после еды. Реже при ахалазии кардии заброс пищи может случаться во сне (так называемая, ночная регургитация): при этом пища нередко попадает в дыхательные пути, что сопровождается «ночным кашлем». Небольшая регургитация характерна для I – II стадии ахалазии кардии, пищеводная рвота – для III – IV стадий, когда происходит переполнение и перерастяжение пищевода.
Боли при ахалазии кардии могут беспокоить натощак или в процессе приема пищи при глотании. Болевые ощущения локализуются за грудиной, часто иррадиируют в челюсть, шею, между лопатками. Если при I – II стадии ахалазии кардии боли обусловлены спазмом мускулатуры, то при III – IV стадии – развивающимся эзофагитом. Для ахалазии кардии типичны периодические приступообразные боли – эзофагодинические кризы, которые могут развиваться на фоне волнения, физической активности, в ночное время и длиться от нескольких минут до одного часа. Болевой приступ иногда проходит самостоятельно после рвоты или прохождения пищевых масс в желудок; в других случаях купируется с помощью спазмолитиков.
Осложнения
Нарушение прохождения пищи и постоянные срыгивания при ахалазии кардии приводят к похуданию, потере трудоспособности, снижению социальной активности. На фоне характерной симптоматики у пациентов развиваются неврозоподобные и аффективные состояния. Нередко больные длительно и безуспешно лечатся у невролога по поводу данных расстройств. Между тем, неврогенные нарушения практически всегда регрессируют после излечения ахалазии кардии.
Диагностика
Кроме типичных жалоб и данных физикального обследования в диагностике ахалазии кардии чрезвычайно важны результаты инструментальных исследований. Обследование пациента при подозрении на ахалазию кардии начинают с обзорной рентгенографии грудной клетки. При выявлении на рентгенограмме тени расширенного пищевода с уровнем жидкости показано проведение рентгенографии пищевода с предварительным приемом бариевой взвеси. Рентгенологическая картина при ахалазии кардии характеризуется сужением конечного отдела пищевода и расширением вышележащего участка, S-образной формой органа.
С помощью эзофагоскопии уточняется стадия и тип ахалазии кардии, наличие и выраженность эзофагита. Для исключения рака пищевода осуществляется эндоскопическая биопсия с последующим морфологическим исследованием биоптата. Для оценки сократительной функции пищевода и тонуса кардиального сфинктера выполняется эзофагеальная манометрия, регистрирующая внутрипищеводное давление и перистальтику. Типичный манометрический признак ахалазии – отсутствие рефлекса раскрытия кардии при глотании.
Ценным диагностическим критерием ахалазии кардии служат результаты фармакологических проб с карбахолином или ацетилхолином: при их введении возникают непропульсивные беспорядочные сокращения мускулатуры в грудном отделе пищевода и усиление тонуса нижнего пищеводного сфинктера, что указывает на денервационную гиперчувствительность органа. Дифференциальный диагноз при ахалазии кардии проводят с доброкачественными опухолями пищевода, эзофагеальными дивертикулами, кардиоэзофагеальным раком, стриктурами пищевода.
Лечение ахалазии кардии
Лечение предусматривает устранение кардиоспазма и может проводиться с помощью консервативных или хирургических методов, иногда – лекарственной терапии. Консервативным методом устранения ахалазии кардии является пневмокардиодилатация – баллонное расширение кардиального сфинктера, которое проводится поэтапно, баллонами разного диаметра с последовательным увеличением давления. С помощью кардиодилатации достигается перерастяжение пищеводного сфинктера и снижение его тонуса. Осложнениями баллонной дилатации могут стать трещины и разрывы пищевода, развитие рефлюкс-эзофагита и рубцовых стриктур кардиального сфинктера.
Стойкий результат лечения ахалазии кардии достигается после хирургического вмешательства – эзофагокардиомиотомии – рассечения кардии с последующей пластикой (фундопликацией). Операция показана при сочетании ахалазии кардии с грыжей пищеводного отверстия диафрагмы, дивертикулами пищевода, раком кардиальной части желудка, безуспешности инструментальной дилатации пищевода, его разрывах.
Если ахалазия кардии сочетается с язвенной болезнью двенадцатиперстной кишки, дополнительно показана селективная проксимальная ваготомия. При наличии тяжелого пептического эрозивно-язвенного рефлюкс-эзофагита и выраженной атонии пищевода производится проксимальная резекция желудка и абдоминальной части пищевода с наложением инвагинационного эзофагогастроанастомоза и пилоропластика.
Лекарственная терапия при ахалазии кардии играет вспомогательную роль и направлена на продление ремиссии. С этой целью целесообразно назначение антидофаминергических препаратов (метоклопрамида), спазмолитиков, малых транквилизаторов, антагонистов кальция, нитратов. В последние годы для лечения ахалазии кардии используется ведение ботулотоксина. Важными моментами при ахалазии кардии служит соблюдение щадящей диеты и режима питания, нормализация эмоционального фона, исключение перенапряжения.
Прогноз и профилактика
Течение ахалазии кардии медленно прогрессирующее. Несвоевременное лечение патологии чревато кровотечением, прободением стенки пищевода, развитием медиастинита, общим истощением. Ахалазия кардии повышает риск развития рака пищевода. После проведения пневмокардиодилатации не исключен рецидив через 6-12 месяцев. Наилучшие прогностические результаты связаны с отсутствием необратимых изменений моторики пищевода и ранним проведением оперативного лечения. Пациентам с ахалазией кардии показано диспансерное наблюдение врача-гастроэнтеролога с выполнением необходимых диагностических процедур.
Ахалазия пищевода
Ахалазия пищевода — это нарушение моторики пищевода, характеризующееся ослаблением перистальтики и неполным расслаблением нижнего пищеводного сфинктера при глотании.
Причины ахалазии пищевода
Причинами могут быть:
- инфекции (бактерии и вирус),
- интоксикация,
- дефицит витамина группы В,
- воспалительные процессы и наружное сдавление пищевода,
- злокачественные новообразования, при которых нарушаются нервные сплетения пищевода,
- тонус и перистальтика пищевода, что приводит к задержке пищи и расширению пищевода.
Большинство пациентов с ахалазией – люди 20-50 лет, в равной мере ахалазия пищевода наблюдается среди мужчин и женщин.
Физиология заболевания. Признаки ахалазии
В норме нижний пищеводный сфинктер находится в состоянии постоянного сокращения. Глотание вызывает возникновение перистальтической волны, которая приводит к кратковременному расслаблению нижнего пищеводного сфинктера.
Трудности во время приема пищи
У больных с ахалазией пищевода прогрессивно увеличивается время, затрачиваемое на прием пищи, они запивают пищу большим количеством жидкости, чтобы улучшить прохождение пищи по пищеводу. Иногда пациенты употребляют шипучие напитки или теплое питье, облегчающие прохождение пищи по пищеводу.
Затруднение глотания
Дисфагия – нарушение акта глотания и затруднение прохождения пищи по пищеводу, развивается постепенно, но иногда возникает остро с эмоциональным напряжением. Сначала развивается затруднение прохождения только твердой пищи, но в более поздних стадиях заболевания развивается затруднение прохождения и жидкой пищи. При этом наблюдаются ощущения давления и тяжести за грудиной, затрудненное дыхание, сердцебиение, может возникнуть удушье, цианоз лица, указывающий на сдавление средостения. Эта ситуация разрешается способом Вильсальвы в положении стоя с отведенной кзади головой, глубокое дыхание, прием большого количества жидкости.
Возможная рвота
Второй частый симптом у пациентов с ахалазий пи щевода – регургирация или пищеводная рвота. Рвотные массы содержат неизмененную пищу и не содержат кислого желудочного сока и желчи. Сначала регургитация проявляется срыгиваниями небольшими порциями, затем рвота становится более обильной (полным ртом), возникает через 2-4 часа после еды, чаще в горизонтальном положении, при наклоне туловища и физических нагрузках. Существует симптом «мокрой подушки», когда рвота появляется ночью, рвотные массы могут попасть в дыхательные пути и вызвать кашель или удушье.
У пациентов с ахалазией пищевода нередко возникают боли распирающего и давящего за грудиной, иррадиирующие в спину, лопатку, шею и напоминают стенокардию.
Похудение
Снижение массы тела наблюдается у 85% пациентов с диагносцированной ахалазией пищевода и является показателем тяжести заболевания, а истощение (кахексия) может явиться причиной смерти. Сочетание выраженной дисфагии и снижение массы тела может имитировать клиническую картину рака пищевода.
Осложнения
Развитие заболевания постепенное, сначала имеются функциональные расстройства без расширения пищевода, затем развивается сужение (стеноз) и расширение пищевода. При длительном течении заболевания могут развиться осложнения в виде воспаления или эрозивно-язвенного процесса в пищеводе, образование дивертикула пищевода, хронический бронхит, воспаление легких.
Ахалазия пищевода. Диагностика
Диагностическими методами для установления диагноза ахалазия пищевода являются:
- рентгенологическое исследование, при котором устанавливается сужение пищевода и расширение его выше места сужения, отсутствие перистальтики нижних отделов пищевода,
- эзофагоскопия для исключения рака пищевода, осложнений ахалазии пищевода, эзофагоспазма, спаек после химических ожогов или травм и т.д.,
- проводится фармакологическая проба с нитроглицерином.
Питание при ахалазии пищевода
Клинических опыт показывает, что временной интервал между появлением клинических симптомов болезни до первичного обращения к врачу варьирует от 1 до 12 лет.
Питание пациентов должно быть механически, химически и термически щадящим, частое дробное питание не менее 4-6 раз в сутки, последний прием пищи за 3-4 часа до сна, после еды полезно выпить стакан теплой воды и побыть вертикально 40-60 минут. Исключаются продукты, усиливающие затруднение прохождение пищи – это мягкие булочные изделия, вареный картофель, фрукты (яблоки, хурма, персики) в свежем виде. Запрещается алкоголь и курение. Спать пациент должен с высоко приподнятым изголовьем.
Ахалазия пищевода. Консервативное и инвазивное лечение
Лечение больных с ахалазией пищевода на ранних стадиях проводится в амбулаторных условиях и включает методы консервативного лечения.
Лекарственная терапия назначается врачом и включает группы следующие препаратов: нитраты, прокинетики, холинолитики и т.д. Назначается также лечебная физкультура, физиотерапевтическое лечение.
Если консервативного лечения недостаточно, то проводится пневматическая баллонная дилятация (расширение) нижнего пищеводного сфинктера.
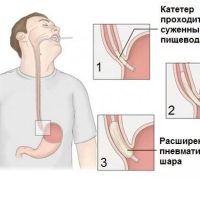
Для этого с помощью баллона, диаметр которого постепенно расширяется, достигают расширения и разрыва круговой мускулатуры кардии и суженного отдела пищевода. Обычно проводят несколько процедур с интервалом 3-4 дня. Основным признаком успешно проведенной дилятации является уменьшение степени дисфагии (затруднения прохождения пищи по пищеводу) и увеличение массы тела.
Хорошие и отличные результаты отмечаются у 60-80% пациентов, причем у пожилых даже более успешно.
Пневматическая дилятация пищевода – менее инвазивный метод и не сопряжен с операционным риском, не осложняется развитием желудочно-пищеводного рефлюкса.
Хирургическое лечение – эзофагокардиомиотомия, резекция кардии и другие варианты хирургического лечения проводятся при малой эффективности расширения пищевода с помощью баллона и при выраженных рубцовых изменениях нижнего пищеводного сфинктера (15-20% больных).
Пациенты с ахалазией пищевода должны находиться на диспансерном наблюдении. Проведение предупредительного и текущего лечения рецидивов и осложнений болезни улучшают ее прогноз.
Ахалазия кардии. Причины, симптомы и лечение
Все перечисленные в заголовке синонимы определяют одно и то же патологическое состояние, но к сердцу, – несмотря на кардиологические корни в некоторых названиях, – эта патология близка разве что по локализации. Речь идет о кардиальном (нижнем, дистальном, конечном) участке пищевода. Этот участок, называемый также кардией, относится к брюшному отделу, который проходит через пищеводное отверстие диафрагмы и далее через клапанный сфинктер сопрягается с желудком.
В ряде источников указывается, что с морфологической точки зрения корректней относить кардию именно к желудку, а не к пищеводу; для простоты будем считать, что кардия – переходная зона между двумя этими органами, протяженность которой сравнительно невелика (несколько сантиметров).
Ахалазией кардии (кардиоспазмом, френоспазмом и т.д.) называют состояние, при котором из-за недостаточного раскрытия сфинктера нарушается проходимость брюшного отдела пищевода, что сопровождается гипотонией и растяжением предлежащих (верхних) отделов. Заболевание описано и известно в медицине давно, со второй половины ХVII века, однако до сих пор остается во многом неясным – прежде всего, в части причин. Кардиоспазм встречается у лиц любого возраста и пола, но пик заболеваемости приходится на зрелую возрастную категорию (старше 30 лет); отмечается незначительное преобладание женщин среди пациентов. Частота встречаемости в пересчете к здоровой популяции специалистами оценивается по-разному и отражает, скорее, готовность региональной выборки обратиться за помощью со специфическими симптомами, нежели истинную распространенность. Однако заболевание в любом случае относится к редким и выявляется у одного человека примерно на 100-200 тысяч населения.
2. Причины
На разных этапах развития медицины выдвигались самые разные гипотезы относительно этиопатогенеза ахалазии кардии. Часть этих гипотез уже однозначно и достоверно опровергнута, другие, кочуя из учебника в учебник, остаются дискутабельными и до сих пор не получают достаточного подтверждения. Примером могут послужить воспалительная, «медленно-инфекционная» и, особенно, психогенная гипотезы. Согласно последней, при определенных психических расстройствах, психотравмах или вариантах личностно-эмоциональной конституции в коре головного мозга могут образовываться очаги застойного возбуждения, вследствие чего ЦНС отдает неверные или избыточные команды, в том числе и блокирующие рефлекторное расслабление кардиального сфинктера. Однако другие авторы не менее убедительно доказывают, что такого рода психические или психологические расстройства являются не причиной, а следствием грубых нарушений работы ЖКТ.
Иногда среди вероятных причин кардиоспазма акцентируют пороки внутриутробного развития, врожденные аномалии иннервации пищеводной мускулатуры и т.п. Предлагается также считать ахалазию кардии полиэтиологическим нейромышечным заболеванием (т.е. таким, которое может развиваться по одному и тому же сценарию под действием любой комбинации из нескольких возможных причин), либо же, наоборот, группой симптоматически сходных заболеваний, у каждого из которых имеется собственный этиопатогенез. Все эти концепции весьма уязвимы для критики, а обсуждаемые потенциальные причины являются, скорее всего, не более чем факторами риска.
Истинные же причины, которыми охватывались и объяснялись бы абсолютно все (или хотя бы важнейшие) клинические, статистические, динамические особенности кардиоспазма, на сегодняшний день неизвестны.
3. Симптомы и диагностика
Несмотря на редкость заболевания, одних только его классификаций, – по самым разным критериям, в т.ч. по доминирующей симптоматике, – существует свыше двадцати пяти. Наиболее типичным симптомом, который обусловлен застойным спазмом нижнего отдела пищевода и аномальным растяжением вышерасположенного грудного отдела (каковое растяжение послужило основой для названия «мегаэзофагус»), является дисфагия – нарушения акта глотания, когда возникают всевозможные дискомфортные ощущения застоя, застревания пищи, переполненности пищевода и т.д. Зачастую такие нарушения носят парадоксальный характер (напр., твердая пища проникает в желудок легче, чем жидкая), что является одним из указаний на нейромышечный дисбаланс, рассогласованность. Другим наиболее распространенным симптомом служит регургитация – обратный интенсивный, активный (в отличие от рефлюкса) выброс пищи в виде отрыжки, срыгивания или рвоты, особенно при наклоне вперед или во время сна («симптом мокрой подушки»). Многие больные интуитивно и небезуспешно стараются предотвратить этот рефлекс «продавливанием» пищи в желудок, для чего задерживают дыхание, выпивают большие объемы воды и т.д. – таким способом создается большое давление в грудном отделе, под влиянием чего пищевые массы преодолевают ограниченно проходимый участок. При дальнейшем прогрессировании заболевания присоединяется загрудинная боль и симптоматика эзофагита (воспаления пищевода), обусловленного постоянным застоем и разложением пищи в мешковидном аномальном расширении. Как правило, утрачивается масса тела, больные жалуются на запах изо рта, жжение, гиперсаливацию (усиленное слюноотделение), слабость, утомляемость и т.д. В некоторых случаях из-за хронической аспирации неестественного содержимого пищевода развиваются осложнения со стороны дыхательной системы.
Диагноз достаточно просто устанавливается по специфической клинической картине и верифицируется рентгенологически.
Дополнительно назначаются ФГДС, эзофагоманометрия и другие исследования по показаниям. Заболевание необходимо дифференцировать от кардиоэзофагеального рака, эзофагеальных стриктур и т.д.
4. Лечение
При своевременном обращении за помощью лечение начинают с консервативных методов. Назначается особая щадящая высококалорийная диета, спазмолитические средства, витаминотерапия и т.д. Применяют различные методики искусственной дилатации (расширения) застойно спазмированного кардиального участка (напр., пневмокардиодилатацию). При отсутствии эффекта и упорном прогрессировании заболевания прибегают к хирургической коррекции, которую некоторые авторы считают методом выбора на любой стадии.
Ультразвуковая диагностика ахалазии кардии
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Ахалазия нижнего пищеводного сфинктера или ахалазия кардии – специфическое заболевание пищевода, основными клиническими проявлениями которого являются дисфагия и регургитация. При этом обычно наблюдаются нарушения транспорта пищи по пищеводу, поскольку перистальтические сокращения последнего отсутствуют, а нижний пищеводный сфинктер не открывается в нужное время или расслабляется недостаточно.
Ахалазия достаточно частое страдание, наблюдающееся у 3,1-20% пациентов с болезнями пищевода [1]. Заболевание, начинающееся исподволь, в любом возрасте, встречает-ся приблизительно одинаково часто как у мужчин, так и женщин. На ранних стадиях диагностика ахалазии трудна даже при эндоскопическом и рентгенологическом исследованиях. Нередко правильный диагноз устанавливается лишь спустя много лет. Больные ахалазией часто направляются на консультацию к психиатру с диагнозом globus hystericus.
Этиология ахалазии до сих пор неизвестна. Некоторые исследователи объясняют развитие заболевания поражением нервных сплетений стенки пищевода или головного мозга. Психический фактор, как основная причина заболевания, отмечается у 38% пациентов [1].
В далеко зашедших случаях ахалазия имеет характерную рентгенологическую симптоматику, позволяющую правильно установить диагноз. При этом пищевод обычно расширен, перистальтические сокращения отсутствуют, а нижний пищеводный сфинктер спастически сокращен (так называемый симптом “мышиного хвостика”).
До последнего времени трансабдоминальное ультразвуковое исследование пищевода считалось невозможным. В 1990 г. Westra и соавт. [2] сообщили о возможности трансаб-доминальной ультразвуковой диагностики гастроэзофагеального рефлюкса и грыжи пищеводного отверстия диафрагмы у детей. В предыдущей публикации [3] мы достаточно подробно описали эхографическую картину аксиальных грыж пищеводного отверстия диафрагмы у взрослых.
Цель этого исследования – разработка ультразвуковой семиотики ахалазии кардии.
Материалы и методы
Ультразвуковое исследование проведено 16 пациентам, находившимся на обследовании и лечении в центре “Гастроэнтерология”, с жалобами на дисфагию и регургитацию. Женщин было-10, мужчин-6, средний возраст обследованных составил 37,6±4,4 года. Исследование проводилось на первый – второй день госпитализации, утром натощак после ночного голодания, на аппарате “SonoET” фирмы “Medison” (Ю. Корея) с использованием конвексного трансдьюсера 3,5 МГц.
Вначале осуществлялось традиционное обследование печени, желчного пузыря, поджелудочной железы, селезенки и желудка. Затем проводилось сканирование в сагиттальной и (или) косой плоскости в эпигастрии, при котором пытались визуализировать пищеводно-желудочное соустье и торакальную часть пищевода. В норме торакальная часть пищевода не видна (рис. 1).
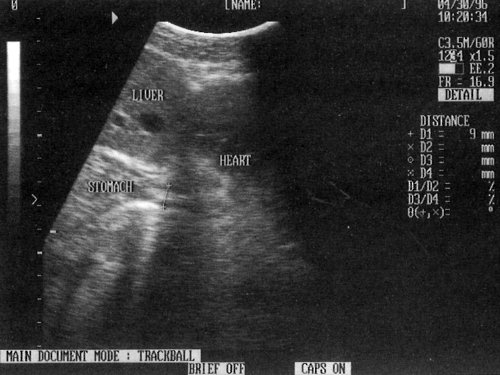
Рис. 1. Ультразвуковое изображение пищевода и желудка в норме (сагиттальный скан, проходящий через пищеводное отверстие диафрагмы).
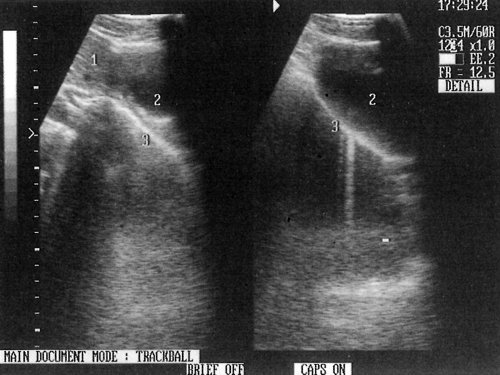
Рис. 2. Сагиттальный скан, проходящий через пищеводное отверстие диафрагмы у пациента с ахалазией (первый тип): 1 – печень, 2 – сердце, 3 – пищевод.
На следующий день после ультразвукового исследования проводилось рентгенологическое исследование пищевода и желудка, при котором диагноз ахалазии устанавливался (отвергался) окончательно.
Результаты исследования
У пятерых пациентов во время ультразвукового исследования торакальную часть пищевода не удалось визуализировать и таким образом не представилось возможным сделать заключение о наличии ахалазии. Однако в трех случаях последующее рентгенологическое исследование выявило заболевание. При этом в грудной полости позади сердца визуализировался расширенный пищевод в виде эхогенного тяжа с несколькими гиперэхогенными включениями в нем (рис. 2). У восьмерых пациентов обнаружена патологическая дилатация пищевода в виде конусоподобной структуры, расположенной позади сердца, с хорошо видимыми стенками шириной 17,1-29,8 мм, заполненной негомогенным мелкодисперсным содержимым, которое перемещалось при перемене положения тела (рис. 3). Во всех этих 11 случаях диагноз ахалазии был подтвержден рентгенологически (рис. 4).
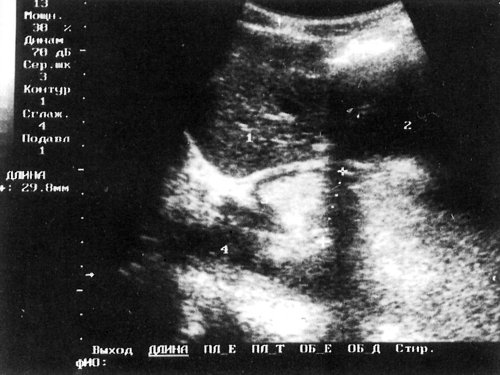
Рис. 3. Сагиттальныи скан, проходящий через пищеводное отверстие диафрагмы, у пациента с ахапазией (второй тип): 1 – печень; 2 – сердце; 3 – расширенный до 29,8 мм пищевод; 4 – аорта.
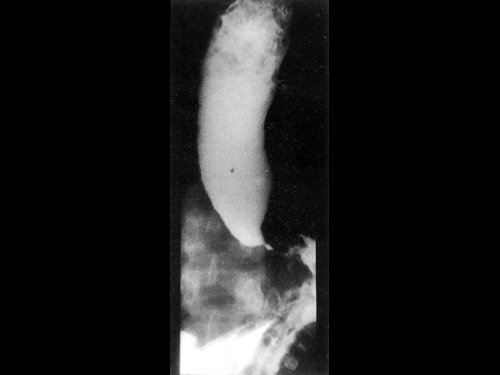
Рис. 4. Рентгенологическое исследование. Пищевод расширен, содержит значительное количество остатков пищи (так называемый симптом “мышиного хвостика”).
Заключение
В нашей предыдущей публикации [3] было показано, что эхография может стать дополнительным инструментальным методом, позволяющим диагностировать аксиальные грыжи пищеводного отверстия диафрагмы. Основываясь на результатах настоящей работы, можно заключить, что трансабдоминальная эхография позволяет диагностировать и ахалазию кардии, и должна использоваться приобследовании пациентов с дисфагией. Но, выявив дилатацию пищевода, необходимо помнить, что она может быть следствием не только ахалазии, но и других заболеваний пищевода, приводящих к ней. К таким заболеваниям относятся, в частности, стеноз пищевода вследствие разрастания опухоли (доброкачественной или злокачественной), желудочно-пищевой рефлюкс пептической стриктуры, рубцовый стеноз, в результате химического или радиационного ожогов. Ультразвуковое исследование должно проводиться, в первую очередь, пациентам, которым рентгенологическое обследование нежелательно (дети, беременные женщины, лица старческого возраста).
Автор приносит искреннюю благодарность сотрудникам СП “Ультрамед-М” (Москва, Россия) Н. Викторову и П. Чупрову за содействие в проведении исследования.
Литература
- Vasilenco VH, Suvorova ТА, Grebenev AL and Achalasia Kardu.// M. Medisina. 1976. – p. 280.
- Ibid.
- Westra SJ, Wolf BHM and Staalman CR. Ultrasound Diagnosis of Gastroesophageal Reflux and Hiatal Hernia in Infants and Young Children PI JCU 1990, – Vol. 18, – pp. 447-480.
- Bourkov SG. Diagnostic Efficacy of Abdominal Ultrasonography in Sliding Gastric and Hiatal Hernias, SonoAce International – 1996, – Vol. 3. – pp. 11-14.

УЗИ сканер HS70
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.