Углеводный обмен
Совокупность процессов, протекающих в организме человека, включающих превращение моносахаридов и их производных, гомо-, гетерополисахаридов и различных углеводсодержащих биополимеров носит название углеводного обмена. Его результатом является снабжение организма энергией, осуществление межмолекулярных взаимодействий и процессов передачи биологической информации.
Этапы углеводного обмена
Процесс включает в себя:
- Пищеварительный этап (переваривание начинается в желудке и заканчивается в тонком кишечнике с участием поджелудочного и кишечного соков, амилазы, лактазы, мальтазы, инвертазы).
- Промежуточный (глюкоза поступает в печень по воротной вене, где происходят гликогенез и неогликогенез, а также гликогенолиз, аналогичные процессы протекают в мышечных тканях).
- Конечный этап (выделение продуктов обмена — воды и углекислого газа из организма).
Причины нарушения углеводного обмена и связанные с ним заболевания
Расстройства метаболизма углеводов делятся:
- на гипогликемии (снижение уровня глюкозы в плазме крови);
- гликогенозы (патологии углеводного обмена врожденного либо наследственного характера, проявляющиеся избыточным накоплением гликогена в клетках организма);
- гексоземии (повышенное содержание гексоз в крови);
- гипергликемии (повышение глюкозы в плазме крови);
- сахарный диабет (нарушения всех звеньев метаболизма углеводов).
Группа нарушений углеводного обмена — гипогликемии, могут быть обусловлены:
- заболеваниями печени (гепатоз, гепатодистрофия, ферментопатии);
- нарушениями пищеварения (проблемы при полостном переваривании углеводов, пристеночном расщеплении и абсорбции);
- болезнями почек (нарушение реабсорбции глюкозы в проксимальных канальцах нефрона);
- эндокринопатиями (глюкокортикоидная недостаточность, дефицит Т3 и Т4, СТГ, катехоламинов, глюкагона);
- углеводным голоданием (из-за нарушений питания);
- длительной и значительной физической работой.
Расстройства углеводного обмена в виде гликогенозов развиваются по причине мутаций генов, которые кодируют синтез ферментов расщепления либо образования гликогена. К таким заболеваниям относят болезнь Гирке, болезнь Помпе, болезнь Андерсена, болезнь Таруи, болезнь Хага и др.
Нарушения углеводного обмена группы гексоземий включают в себя галактоземию врожденного или наследственного характера, а также фруктоземию с врожденной непереносимостью фруктозы, возникающую по причине недостаточности альдолазы В.
Гипергликемии — расстройства углеводного обмена, которые развиваются по таким причинам:
- эндокринопатии (избыток эффектов гипергликемизирующих факторов и дефицит эффектов инсулина);
- психогенные и неврологические расстройства (психическое возбуждение, стресс-реакции, каузалгии);
- переедание (долгое избыточное употребление сладостей и легкоусвояемых углеводов);
- патологии печени (печеночная недостаточность).
Сахарный диабет — распространенное нарушение углеводного обмена. Подразделяется на инсулинзависимый и инсулиннезависимый. Причинами сахарного диабета считаются:
- дефицит инсулина (генетические дефекты β-клеток островков Лангерганса; вирусы, тропные к β-клеткам; иммунные факторы; эндогенные токсические вещества; воспалительные процессы; физические и химические факторы);
- недостаточность эффектов инсулина (нейро- или психогенных факторы; контринсулярных факторы; дефекты инсулиновых рецепторов и пострецепторные нарушения в клетках-мишенях).
Лечение и профилактика нарушений углеводного обмена
Терапия направлена на нормализацию метаболизма углеводов в организме. Лечение разрабатывается индивидуально исходя из типа и выраженности патологии углеводного обмена.
Профилактика нарушений метаболизма заключается в правильном сбалансированном питании, своевременном лечении возникающих заболеваний печени, почек, эндокринных желез.
Узнать индивидуальные риски по развитию болезней, связанных с углеводным обменом, позволяет генетическое тестирование. В медико-генетическом центре «Геномед» можно пройти исследование «Наследственные нарушения обмена веществ».
Гликогенозы ( Болезнь накопления гликогена , Гликогеновая болезнь )
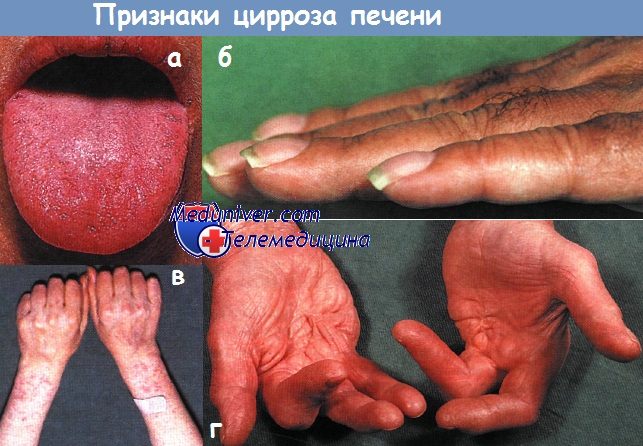
Гликогенозы – наследственные болезни, в основе которых лежит генетический дефект производства ферментов, принимающих участие в метаболизме углеводов. Характерный общий признак – чрезмерное отложение гликогена в миоцитах, гепатоцитах и других клетках организма. Гликогенозы проявляются симптомами гипогликемии, гепатомегалии, мышечной слабости, печеночной, сердечной, дыхательной и почечной недостаточности. Диагностика включает биохимический анализ крови, морфологическое исследование биопсийного материала мышц и печени, определение активности ферментов, молекулярно-генетические тесты. Лечение основано на лечебном питании, медикаментозной коррекции метаболических расстройств, в ряде случаев требуются операции.
МКБ-10
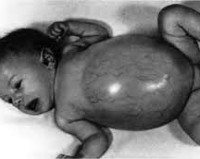
Общие сведения
Исследование гликогенозов ведется с 1910 года. В 1928-29 годах была описана симптоматика гликогеноза I типа – «болезни накопления гликогена». Лишь в 1952 году удалось выявить ферментный дефект и установить его связь с развитием симптомов. Патогенетические механизмы и способы лечения до сих пор остаются не до конца изученными. К настоящему времени выделено 12 типов гликогенозов, наиболее полно исследовано 9. Распространенность низкая, в среднем составляет 1 случай на 40-68 тысяч населения. Эпидемиологические показатели одинаковы среди представителей обоих полов, но при X-рецессивном наследовании мужчины болеют чаще. Симптомы проявляются в период новорожденности или в раннем детстве, течение чаще непрерывно прогрессирующее.

Причины гликогенозов
Единственным фактором, провоцирующим развитие гликогеновых болезней, является генетический дефект, в результате которого возникает недостаточность определенного фермента, участвующего в обмене глюкозы. Все гликогенозы за исключением IX типа наследуются по аутосомно-рецессивному принципу. Это означает, что мутационный ген расположен на хромосоме, не сцепленной с полом, проявление заболевания возможно только при наследовании мутаций от каждого из родителей – при наличии двух рецессивных измененных генов в аллели. Если дефектным является один ген из пары, то другой – доминантный, нормальный – обеспечивает организм достаточным количеством фермента. Человек при этом становится носителем гликогеноза, но не болеет. В парах, где оба партнера – носители, вероятность рождения больного ребенка составляет 25%. При гликогенозе типа IX патологический ген локализован в половой X-хромосоме. Гемизиготные мужчины имеют пару XY, всегда больны гликогенозом, передают дефект всем своим дочерям. Вероятность передачи мутации от женщины-носительницы детям обоих полов составляет 50%.
Патогенез
Патогенетическая основа всех гликогенозов – невозможность процесса синтеза и распада гликогена, его накопление в тканях. Гликоген является единственным резервным полисахаридом организма, своеобразным энергетическим «депо» – после приема пищи излишек глюкозы превращается в гликоген печени и мышц, затем постепенно расщепляется обратно до глюкозы. Благодаря этому механизму поддерживается стабильный уровень сахара в плазме крови, клетки и ткани организма непрерывно обеспечиваются энергией. При агликогенозе (0 тип) – отсутствует фермент гликогенсинтетаза, ответственная за производство гликогена. Пациенты страдают от тяжелой гипогликемии.
При гликогеновых болезнях типов 1-11 возникает генетически обусловленная недостаточность какого-либо фермента, катализирующего цепочку глюкоза-гликоген-глюкоза. 1 тип характеризуется дефектом глюкозо-6-фосфатазы и глюкозо-6-фосфаттранслоказы, 2 тип – альфа-1,4-глюкозидазы, 3 тип – амило-1,6-глюкозидазы, 4 тип – D-1,4-глюкано-α-глюкозилтрансферазы, 5 тип – гликогенфосфорилазы миоцитов, 6 тип – крахмалфосфорилазы гепатоцитов, 7 тип – фосфоглюкомутазы, 8 тип – фосфофруктомутазы, 9 тип – киназы фосфорилазы гепатоцитов. Из-за сниженной активности или полного отсутствия фермента гликоген накапливается в мышцах, печени, редко – в других тканях. Изменяется структура и функциональность органов, развиваются различные формы органной недостаточности.
Классификация
С учетом ферментативного дефекта и особенностей клинических проявлений выделяют 12 вариантов гликогенозов, от 0 до XI. Кроме того, описаны случаи комбинированных типов, когда определяется дефицит двух ферментов, а также случаи неидентифицируемых типов, при которых выделить ферментный дефект не удается. Согласно ведущему патогенетическому механизму гликогеновые болезни подразделяются на три больших группы:
- Печеночные. Включают гликогенозы всех типов, кроме II, V и VII. Гликоген откладывается преимущественно в гепатоцитах. Характерна гепатомегалия, гипогликемия через 2 часа после поступления углеводов. При I типе заболевания также поражаются почки, при III и IV типах развиваются миопатии.
- Мышечные. В данную группу входят болезни типов VII и V. Изменена ферментативная активность в мышечной ткани, нарушено энергообеспечение мышц. Типичные симптомы – миалгии, судороги.
- Смешанные. Гликогеноз II типа отличается тем, что в патологический процесс вовлекаются все гликогенсодержащие ткани. Гликоген скапливается в лизосомах и цитоплазме клеток. Страдают многие органы, возрастает риск смерти по причине сердечной или дыхательной недостаточности.
Симптомы гликогенозов
Агликогеноз развивается в периоде новорожденности либо раннего детства. Низкое содержание гликогена в печени проявляется резко выраженной гипогликемией натощак. Наблюдается заторможенность, глубокий сон, потеря сознания, бледность кожи, тошнота, рвота, судороги ночью и в утренние часы. Внешне пациенты низкорослые, имеют пониженную плотность костной ткани, повышенный риск переломов. При болезни Гирке (I тип) симптомы дебютируют в первые 4 месяца жизни. Характерен плохой аппетит, приступы рвоты, недостаток веса, увеличение печени, диспропорциональность строения тела – круглое лицо, большой живот, тонкие конечности.
Клинические признаки болезни Помпе (II тип) определяются в течение нескольких недель после рождения. Дети вялые, малоподвижные, с ослабленным сосательным рефлексом, сниженным аппетитом. Гепатомегалия изменяет пропорции тела – живот увеличивается, руки и ноги остаются тонкими. Поражается сердце, легкие, нервная система. Высок риск сердечной и легочной недостаточности. У пациентов с болезнью Форбса (III тип) симптомы слабой и умеренной выраженности. На первый план выходит гипогликемия постабсорбционного периода, гепатомегалия, накопление подкожного жира в области туловища. Ведущие симптомы болезни Андерсена (IV тип)– мышечная слабость, плохая переносимость физической нагрузки, судороги.
Болезнь Томсона представлена гепатомегалией, нистагмом, атаксией, прогрессирующими неврологическими нарушениями с мышечной гипертонией, децеребрацией. Типичные проявления болезни Мак-Ардля (V тип) – боли, спазматические сокращения, чрезмерная утомляемость и слабость мышц даже после незначительной нагрузки. Иногда тонические судороги переходят в генерализованные, что сопровождается общей скованностью. Проявления болезни Герса (VI тип) менее выраженные, пациенты способны переносить легкие и умеренные физические нагрузки, не испытывая дискомфорта. Дополнительно обнаруживаются признаки поражения печени – угнетение аппетита, рвота, тошнота, боли в правом боку.
Течение болезни Таруи (VII тип) включает непереносимость физической нагрузки, сопровождающуюся тошнотой и рвотой, болезненными спазмами мышц. Поступление глюкозы не повышает способность совершать физические действия. После употребления пищи симптомы обостряются. Наиболее мягкое течение свойственно болезни Хага (IX тип). У больных детей увеличивается печень, задерживается моторное развитие и рост, формируется мышечная гипотония. С возрастом симптомы самостоятельно редуцируются. Гликогеноз X типа крайне редок, характеризуется гепатомегалией, при длительном течении снижается переносимость физических нагрузок. Гликогеноз XI типа сопровождается значительным увеличением печени, задержкой роста и физического развития, рахитом. У подростков нередко наблюдается сокращение объема печени, ускорение роста.
Осложнения
При разновидностях гликогенозов, сопровождающихся гипогликемией, существует риск развития гипогликемической комы. Как правило, выраженное снижение уровня глюкозы в крови происходит при пропуске приемов пищи, особенно после ночного сна (пропуск завтрака). Пациенты испытывают головокружение и судороги, теряют сознание. Тяжелые формы мышечных гликогенозов при продолжительном течении и отсутствии терапии приводят к дистрофии скелетных мышц, сердечной недостаточности. Осложнением некоторых печеночных гликогенозов является цирроз печени.
Диагностика
При подозрении на гликогеноз ребенку рекомендуется консультация врача-генетика, педиатра, гастроэнтеролога, гепатолога. В первую очередь специалист собирает анамнез, проводит клинический опрос и осмотр. Поскольку заболевание передается аутосомно-рецессивным способом, семейные случаи выявляют редко. Распространены жалобы на слабость, апатичность ребенка, бледность и желтушность кожи, отказ от еды или повышенный аппетит, трудности пробуждения утром, тремор, судороги. При осмотре врач отмечает увеличение размера печени, выпирание живота, задержку роста, мышечную гипотрофию, специфическое отложение подкожной жировой клетчатки, ксантомы. Лабораторные и инструментальные методы позволяют подтвердить диагноз гликогеноза, исключить врожденный сифилис, токсоплазмоз, цитомегалию, патологии печени, болезнь Гоше, миотонию, прогрессирующую мышечную дистрофию, амиотрофии. К обязательным методам исследований относят:
- Биохимическое исследование крови. По результатам анализа обнаруживается гипогликемия с уровнем глюкозы натощак 0,6-3 ммоль/л, лактатацидоз с концентрацией молочной кислоты 3-10 ммоль/л (кроме гликогеноза 4 типа). Дополнительно выявляется увеличение показателей триглицеридов, общего холестерина, ЛПНП, ЛПОНП, мочевой кислоты, печеночных ферментов.
- Исследование биоптата печени, мышц. При изучении ткани печени наиболее распространенными характеристиками являются повышенное количество гликогена и его глыбчатое распределение в цитоплазме гепатоцитов, иногда – в вакуолизированных ядрах. Определяется выраженная белковая и/или крупно- и мелкокапельная жировая дистрофия гепатоцитов, их некроз, ограниченные очаги фиброза в местах гибели клеток. Возможны признаки цирроза. При мышечных типах болезней исследуется мышечный биоптат, в котором просматриваются субсарколеммальные накопления структурно нормального гликогена.
- Исследование ферментов. Активность ферментов изучается в культуре кожных фибробластов, биоптате мышечной и печеночной ткани, лейкоцитах. При гликогенозах с хроническим медленно прогрессирующим течением снижение функциональности фермента легкое или умеренное. При тяжелом течении фермент отсутствует либо его активность минимальна.
- УЗИ брюшной полости. Отмечается выраженное увеличение печени, особенно левой ее доли. Характерна гиперэхогенность и структурная диффузная неоднородность паренхимы (множественные мелкие гиперэхогенные эхосигналы, распределенные равномерно). В дистальных отделах паренхимы прохождение ультразвука ослаблено. Возможно обнаружение структурно разнообразных печеночных аденом, увеличение размеров почек, селезенки и поджелудочной железы.
Комплекс диагностических исследований подбирается индивидуально в зависимости от возраста пациента и предполагаемого типа гликогеновой болезни. Может потребоваться молекулярно-генетическая диагностика (секвенирование генов с целью выявления мутации), электромиография, ЭХО-КГ, ОАК, коагулограмма.
Лечение гликогенозов
Специфические методы терапии не разработаны. Патогенетическое лечение проводится консервативно, направлено на устранение гипогликемии, метаболического ацидоза, кетоза, гиперлипидемии, коррекцию дисфункции гепатобилиарного комплекса и желудочно-кишечного тракта. При развитии осложнений (серьезном поражении внутренних органов) выполняются хирургические операции. Медицинская помощь пациентам включает следующие направления:
- Диетотерапию. Для минимизации метаболических нарушений составляется индивидуальный план питания. Больным рекомендуется снизить количество жиров, сахарозы, фруктозы и галактозы для уменьшения гиперлипидемии и ацидоза. При первом типе гликогеноза назначается диета с увеличенным потреблением углеводов. В частности, показано употребление сырого кукурузного крахмала с медленной усвояемостью, позволяющей предупредить гипогликемию. При типах 3, 4 и 9 вводится рацион с преобладанием животного белка и дробным питанием.
- Лекарственную коррекцию симптомов. В рамках комплексного лечения применяется кокарбоксилаза для увеличения производства ацетилкофермента А, кортикостероидов и глюкагона для стимуляции глюконеогенеза. Дефицит карнитина компенсируется левокарнитином. При вторичных тубулопатиях, печеночных и билиарных дисфункциях используются желчегонные препараты, гепатопротекторы, липотропные вещества. При признаках ацидоза показаны щелочные растворы внутривенно. При почечной дисфункции, протеинурии – ингибиторы АПФ. При гиперурикемии – урикодепрессоры. При нейтропении – гранулоцитарный колониестимулирующий фактор.
- Хирургическое лечение. Пациентам с тяжелыми фатальными поражениями печени может потребоваться ортотопическая трансплантация органа. Показанием к операции является цирроз с осложнениями, часто развивающийся при третьем и четвертом типе патологии. В отдельных случаях хирургическое вмешательство целесообразно при аденомах печени с высоким риском трансформации в злокачественную опухоль. Трансплантация почек иногда выполняется больным с хронической почечной недостаточностью.
Прогноз и профилактика
Эффективность терапии, вероятность осложнений и летального исхода зависят от типа патологии. Одни гликогенозы незначительно ухудшают качество жизни больных, компенсируются по мере взросления, другие – не поддаются лечению и неизбежно завершаются смертью. Для снижения риска рождения ребенка с гликогенозом супружеским парам из группы риска – имеющим семейный отягощенный анамнез, детей с подтвержденным диагнозом – требуется медико-генетическое консультирование, пренатальная диагностика.
Патогенез гликогенозов
- Главная /
- Редкие болезни /
- Энциклопедия заболеваний /
- ГЛИКОГЕНОЗ I ТИПА
(GLYCOGEN STORAGE DISEASE I, VON GIERKE DISEASE, HEPATORENAL FORM OF GLYCOGEN STORAGE DISEASE)
GLYCOGEN STORAGE DISEASE Ia GLUCOSE-6-PHOSPHATASE DEFICIENCY OMIM +232200
GLYCOGEN STORAGE DISEASE Ib GLUCOSE-6-PHOSPHATE TRANSPORT DEFECT OMIM #232220
Генетика: Гликогеноз I типа разделяют на две формы – Ia и Ib типов, которые обусловлены мутациями в разных генах и несколько различаются клинически. Мутации гена глюкозо-6-фосфатазы (G6PC) обуславливают гликогеноз Iа, мутации гена транспортного белка глюкозо-6-фосфата (G6PТ1, OMIM *602671) обуславливают гликогеноз Ib. Ген G6PC картирован на 17q21. Ген G6PТ1 картирован на 11q23 .
Тип наследования: аутосомно-рецессивный.
Частота: Относится к числу редких наследственных болезней обмена веществ. Частота заболевания 1: 50 000- 1: 100 000 живых новорожденных. Патогенез: Глюкозо-6-фосфатаза катализирует конечную реакцию и глюконеогенеза, и гидролиза гликогена, и осуществляет гидролиз глюкозо-6-фосфата на глюкозу и неорганический фосфат. Транспортный белок осуществляет перенос субстрата через мембрану эндоплазматического ретикулума.
Клинические проявления: Заболевание чаще всего дебютирует на 3-4 месяцах жизни. Основными симптомами являются гепатомегалия и гипогликемия. При осмотре у детей отмечается увеличения размеров печени, локальные отложения жира, преимущественно на щеках (“кукольное” лицо), ягодицах, бедpах, мышечная гипотрофия и задержка роста. Могут возникать кожные ксантомы на локтях, коленях, ягодицах, бедpах. Тяжелая гипогликемия и лактатацидоз провоцируются задержками в кормлении и интеркуррентными инфекциями. Несмотря на значительное увеличение размеров, функция печени, как правило, не страдает. На втором- третьем десятилетии жизни могут появляться аденомы печени, имеющие склонность к злокачественному пеpеpождению. У большинства больных с гликогенозом Ib типа развивается нейтропения до 1 года жизни. Этим обьясняется склонность к инфекциям (рецидивирующие отиты, стоматиты, гингивиты, пневмонии, инфекции респираторного тракта, инфекции мочевого тракта и др.). Примерно у 75% больных с Ib типом развиваются язвы слизистой кишечника, хроническое воспаление кишечника.
Диагностика: Основными методами подтверждения диагноза являются биохимические (определение активности фермента глюкозо-6-фосфатазы в биоптате печени) и молекулярно-генетические (выявление мутаций в генах G6PC и G6PT1). Диагностика проводится в лаборатории наследственных болезней обмена веществ МГНЦ РАМН (http://www.labnbo.narod.ru).
Лечение: основная цель лечения – предотвращение гипогликемии и вторичных метаболических нарушений. Первоначально рекомендации по лечению включали только частые кормления с повышенным содержанием углеводов, однако это не всегда позволяло поддерживать нормальный уровень глюкозы в течение суток. Поэтому детям младшего возраста с тяжелой гипогликемией, помимо частых дневных кормлений, показано проведение ночных вскармливаний через назогастральный зонд, что обеспечивает нормальный уровень глюкозы в крови, а также полноценный ночной сон пациентам и их родителям. Всем больным назначается диета с высоким содержанием углеводов: углеводы – 65-70%, белки – 10-15%, жиры – 20-25%., частые кормления. Для увеличения интервала между приемами пищи применяют сырой кукурузный крахмал (для детей старше 1 года). Начальная доза составляет 0,25 г/кг массы тела и должна увеличиваться медленно для предупреждения побочных эффектов со стороны желудочно-кишечного тракта. Пациентам с формой Ib при выраженной нейтропении назначают гранулоцит-стимулирующий фактор (препараты «Граноцит», «Нейпоген»). Пациенты обычно хорошо отвечают на лечение малыми дозами (начальная доза 2.5 ?г/кг через день). Прогноз в большинстве случаев благоприятный. В случаях плохой коррекции метаболических нарушений методами диетотерапии при гликогенозе I типа показана трансплантация печени.
Гликогеноз
Организм человека имеет энергетический резерв. Одним из соединений, исполняющих данную роль, является гликоген, который способен быстро распадаться на простейшую глюкозу, питая при этом организм энергией. Печень расщепляет гликоген и трансформирует с помощью определенных ферментов. При недостатке этих специфических ферментов гликоген накапливается в печеночной паренхиме и мышечной ткани. Эта патология называется гликогенозом. Заболевание носит наследственный по рецессивному типу характер и развивается по причине генетической мутации.
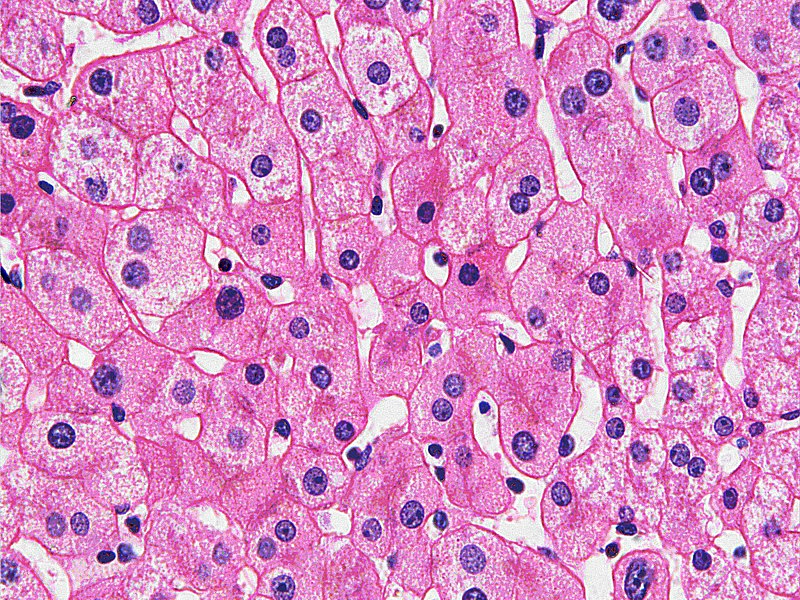
Печеночная форма гликогеноза
Данная форма заболевания характеризуется локализацией патологического процесса в соответствующем депонирующем органе.
Течение болезни. Заболевание начинает себя проявлять с 8–9-го месяца жизни. До этого времени ребенок развивается нормально или немного замедленно. Первые признаки характеризуются непроизвольным сокращением мышц конечностей, временной потерей сознания. Приступы гипогликемии наблюдаются в основном утром или в большом промежутке времени между приемами пищи. Их появление можно предотвратить приемом сладкой воды. Осложнить течение гликогеноза могут интеркуррентные заболевания (инфекционные процессы). Первые пять лет считаются наиболее опасными для жизни. С возрастом состояние больного улучшается за счет развития компенсаторных механизмов и реакций приспособления. На умственные способности гликогенозы негативного воздействия не оказывают.
Симптомы. Симптоматические патологии проявляются в различной степени тяжести и зависят от ряда факторов, в том числе от вида недостающего фермента, участвующего в обмене глюкозы. Наиболее характерными считаются следующие симптомы: увеличение печени, селезенки, потеря аппетита, аномалии мышечного тонуса, замедленное физическое развитие, воспаление суставов, высокая утомляемость, образование камней в почках, множественные поражения центральной нервной системы, ощущение затруднения дыхания, увеличение размеров сердца и другие.
Диагностика. При физикальном осмотре врач уделяет особое внимание размеру печени. Если констатируется факт ее увеличения, необходимо сдать кровь и мочу на анализы, чтобы комплексно исследовать липидный обмен, уровень глюкозы. Обязательно проводятся гематологическое и молекулярно-генетическое исследования, позволяющие проанализировать активность ферментов и выявить наличие гликогена в тканях. ДНК-диагностика выявляет мутированные гены.

Лечение. Лечение может быть назначено только врачом. Оно обычно состоит из соблюдения диеты и заместительной терапии. Рацион должен включать до 8 приемов пищи в день (включая ночное время). Метод заместительной терапии направлен на восполнение недостающих компонентов в организме для его нормальной жизнедеятельности.
Фосфоглив* —

1. Настоящая информация основана на исследованиях, проводимых ООО «Ипсос Комкон», и действительна по состоянию на декабрь 2016 года
2. Распоряжение правительства РФ от 28 декабря 2016 г. № 2885-р «Об утверждении перечней жизненно необходимых и важнейших лекарственных препаратов для медицинского применения на 2017 год»
3. Ивашкин В.Т., Бакулин И.Г., Богомолов П.О., Мациевич М.В. и др., 2017 г.
4. Бакулин И.Г., Бохан Н.А., Богомолов П.О., Гейвандова Н.И. и др., 2017 г.
5. Буеверов А.О., 2014 г.
6. Филимонкова Н.Н., Воробьева Ю.В., Топычканова Е.П., 2013 г.
7. Новикова Т.И., Новиков В.С., 2011 г.
8. Приказ МЗ РФ от 10.11.2011 г. № 1340н «Об утверждении Перечня лекарственных средств, отпускаемых по рецептам врача (фельдшера) при оказании дополнительной бесплатной медицинской помощи отдельным категориям граждан, имеющим право на получение государственной социальной помощи»
9. Приказ Минздрава РФ от 09.11.2012 N 772н «Об утверждении стандарта специализированной медицинской помощи при других заболеваниях печени»
10. Инструкция по медицинскому применению
11. И.Г. Никитин, И.Е. Байкова, В.М. Волынкина и соавторы, 2009г.
12. Ивашкин В.Т., Драпкина О.М., Маев И.В. и др. Распространенность неалкогольной жировой болезни печени у пациентов амбулаторно-поликлинической практики в Российской Федерации: результаты исследования DIREG 2 //РЖГГК. – 2015. – № 6. – С. 31-41
Патогенез гликогенозов
Саратовский государственный медицинский университет им. В.И. Разумовского Росздрава, НИИ фундаментальной и клинической уронефрологии Саратовского ГМУ
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
Медико-генетический центр РАМН
НИИ детской эндокринологии Эндокринологического научного центра, Москва
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
ФГБУН «Федеральный исследовательский центр питания, биотехнологии и безопасности пищи», Москва, Россия
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
Гликогеноз IX типа у ребенка 9 лет
Журнал: Проблемы эндокринологии. 2017;63(2): 139-142
Болотова Н. В., Аверьянов А. П., Филина Н. Ю., Захарова Е. Ю., Меликян М. А., Великоцкая О. А., Строкова Т. В., Пальцева Ю. В. Гликогеноз IX типа у ребенка 9 лет. Проблемы эндокринологии. 2017;63(2):139-142.
Bolotova N V, Averyanov A P, Filina N Yu, Zakharova E Iu, Melikian M A, Velikotskaya O A, Strokova T V, Paltseva Y V. Glycogenosis type IX in a 9-year-old child. Problemy Endokrinologii. 2017;63(2):139-142. (In Russ.).
https://doi.org/10.14341/probl2017632139-142
Саратовский государственный медицинский университет им. В.И. Разумовского Росздрава, НИИ фундаментальной и клинической уронефрологии Саратовского ГМУ





У ребенка с 1 года отмечались гипогликемические состояния, сопровождающиеся кетозом, периодические гипергликемии, по поводу чего поступил в детское эндокринологическое отделение КБ им. С.Р. Миротворцева Саратова. В стационаре ребенку было проведено комплексное обследование, по результатам которого были исключены такие заболевания, как гиперинсулинизм, сахарный диабет. В лаборатории наследственных болезней обмена веществ ФГБНУ «Медико-генетический научный центр» была выявлена гемизиготная мутация в гене РНКА2 (гликогеноз IX типа). У матери также выявлена гетерозиготная мутация с.226G>А(р.Е76К в гене РНКА2. По результатам проведенного генетического обследования ребенка и матери пациенту был выставлен окончательный диагноз: гликогеноз IX типа. Пациенту была назначена индивидуальная персонализированная белковая диета с исключением пищевого сахара, жирных продуктов, рекомендован кукурузный крахмал — 30 г через каждые 6 ч и на ночь. На фоне строгого соблюдения диеты приступы стали реже, тяжесть приступов уменьшилась.
Саратовский государственный медицинский университет им. В.И. Разумовского Росздрава, НИИ фундаментальной и клинической уронефрологии Саратовского ГМУ
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
Медико-генетический центр РАМН
НИИ детской эндокринологии Эндокринологического научного центра, Москва
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
ФГБУН «Федеральный исследовательский центр питания, биотехнологии и безопасности пищи», Москва, Россия
ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского», Саратов, Россия
В настоящее время отмечается рост болезней обмена веществ. Большую группу заболеваний представляют гликогенозы, включающие 15 известных на данный момент типов. Гликогенозы — группа достаточно редких наследственных заболеваний, связанных с дефектами различных ферментов, необходимых для синтеза и распада гликогена. Гликогенозы встречаются в среднем с частотой 1 случай на 40 000—68 000 населения. Прогноз у каждого вида гликогеноза свой: некоторые имеют благоприятное течение, и больные доживают до старости, другие заканчиваются летально в детском возрасте.
Описание случая
Мальчик впервые поступил в детское эндокринологическое отделение КБ им. С.Р. Миротворцева Саратова в июле 2015 г. в возрасте 7 лет с жалобами на периодические приступы слабости, потливости, тремор, судороги, сопровождающиеся чувством голода.
Из анамнеза жизни известно, что ребенок от 3-й беременности (1-я закончилась рождением здоровой девочки, 2-я — медицинским абортом), протекавшей на фоне угрозы прерывания на 10-й и 24-й неделях гестоза I и II триместров. Роды срочные путем кесарева сечения на фоне обвития пуповиной. Длина тела при рождении 51 см, масса 2900 г. С рождения отмечались высокие темпы роста: 5—6 см, прибавки массы тела 2—2,5 кг ежемесячно. Рост в 1 год составлял 82 см, масса — 12 300 г. Наследственность отягощена по линии матери: у дедушки и его родного брата, у прабабушки с раннего детства отмечались гипогликемические состояния. У дедушки и родной сестры бабушки — сахарный диабет 2-го типа.
У ребенка с 1 года отмечались приступы слабости, потливости, тремор, судороги, сопровождавшиеся чувством голода (чаще после ночного сна и после физической нагрузки), купировавшиеся приемом легкоусвояемых углеводов. Подобные состояния сопровождались кетонурией. Ребенок трижды обследовался в педиатрическом стационаре по месту жительства с подозрением на эпилепсию. Диагноз был исключен. За 3 мес до поступления в детское эндокринологическое отделение у ребенка отмечалось гипогликемическое состояние с потерей сознания — гликемия составляла 1,1 ммоль/л. Периодически отмечались повышения гликемии, максимально до 19,6 ммоль/л. Для уточнения причины нарушения углеводного обмена ребенок был направлен в детское эндокринологическое отделение КБ им. С.Р. Миротворцева.
При поступлении: рост 138 см, масса тела 28 кг, ИМТ 14,2 кг/м 2 . SDS роста 1,55. Физическое развитие выше среднего (соответствует 10 годам) гармоничное. Костно-мышечная система без особенностей. Мышечная сила достаточная. Кожные покровы чистые бледные. Видимые слизистые розового цвета. Дыхание в легких везикулярное, хрипы не выслушиваются. Тоны сердца ясные ритмичные. Живот мягкий, доступен глубокой пальпации, безболезненный во всех отделах. Печень определяется по краю реберной дуги. Физиологические отправления без особенностей. Нервно-психическое развитие: ребенок в сознании, ориентирован во времени и пространстве, на вопросы отвечает адекватно, развит по возрасту.
За время госпитализации у мальчика многократно были зафиксированы гипогликемические состояния с минимальным уровнем гликемии 2,1 ммоль/л. Приступы гипогликемии сопровождались кетозом, неукротимой рвотой, тахикардией до 140 уд/мин.
Для исключения гиперинсулинизма ребенку была проведена голодовая проба. Минимальный уровень гликемии составил 2,6 ммоль/л, голодный промежуток — 12 ч. В момент гипогликемии ИРИ 0,8 мМЕ/мл, С-пептид 0,18 нг/мл. Результаты голодовой пробы, ацетонемические состояния на фоне гипогликемии позволили предположить, что гипогликемические состояния не связаны с гиперинсулинизмом. Также у ребенка за период наблюдения в стационаре трехкратно были зафиксированы эпизоды гипергликемии — максимально до 18,9 ммоль/л, отмечалось ацетонемическое состояние — многократная рвота, ацетонурия. Уровень сахара крови самостоятельно снижался до нормогликемии без введения инсулина. Глюкозурия зафиксирована не была. Для исключения сахарного диабета ребенку был проведен пероральный глюкозотолерантный тест: гликемия натощак 3,09 ммоль/л, ИРИ 2 мМЕ/мл, С-пептид 0,45 нг/мл. Через 1 ч: гликемия 4,77 ммоль/л, ИРИ 33,2 мМЕ/мл, С-пептид 5 нг/мл. Через 2 ч: гликемия 5,28 ммоль/л, ИРИ 39,6 мМЕ/мл, С-пептид 5 нг/мл. Антитела к инсулину, глутаматдекарбоксилазе, бета-клеткам поджелудочной железы отсутствовали. Отсутствие гипергликемии на фоне углеводной нагрузки, отсутствие глюкозурии, а также отрицательный титр аутоантител позволили на данном этапе диагностического поиска исключить сахарный диабет. Ребенок был выписан с диагнозом: нарушение углеводного обмена, гипогликемии неясного генеза.
Образец крови ребенка был направлен в Эндокринологический научный центр Москвы, где при проведении генетического обследования были выявлены 2 гетерозиготные мутации: pE750Q (rs201996097) в гене RFX6 и p. A3V (rs/146089816) в гене PTF1A.
Патологическая значимость мутаций неизвестна, но оба гена отвечают за работу бета-клеток поджелудочной железы.
Через 6 мес ребенок повторно поступил в КБ им. С.Р. Миротворцева в связи с учащением гипогликемических состояний. Для уточнения диагноза пробы крови и мочи ребенка были отправлены в Лабораторию наследственных болезней обмена веществ Москвы. При исследовании органических кислот и кетоновых тел в моче, ТМС (аминокислоты, ацилкарнитины) получен отрицательный результат.
Тем временем у ребенка участились приступы гипогликемий (до 2—3 раз в неделю), сопровождающиеся неукротимой рвотой и кетоацидозом, часто с потерей сознания. При повторном стационарном обследовании в детском эндокринологическом отделении КБ им. С.Р. Миротворцева через полгода после последней госпитализации у ребенка была выявлена гепатомегалия (правая доля 121 мм, левая 78 мм), уровень трансаминаз при этом соответствовал норме.
Ребенок был направлен в Лабораторию наследственных болезней обмена веществ ФГБНУ «Медико-генетический научный центр», где при проведении генетического анализа методом таргентного секвенирования (проведен анализ 47 генов) была выявлена гемизиготная мутация в гене РНКА2 (гликогеноз IX типа). У матери пациента выявлена мутация с.226G>А (р.Е76К) в гене РНКА2 в гетерозиготном состоянии. Мать пробанда является носителем мутации. По результатам генетического исследования пациенту был выставлен окончательный диагноз — гликогеноз IX типа. Молекулярно-генетическое исследование проведено в рамках программы «Альфа-Эндо».
После получения результатов молекулярно-генетического обследования ребенок находился в Эндокринологическом научном центре Москвы с 13.12.16 по 19.12.16, где получал специализированное лечение. Для определения дальнейшей программы лечения ребенок был консультирован специалистами клиники ФГБУН «ФИЦ питания и биотехнологии». Назначена индивидуальная персонализированная диета при гликогеновой болезни с исключением пищевого сахара, жирных продуктов, включающая значительное содержание белка, рекомендован кукурузный крахмал — 30 г через каждые 6 ч и на ночь.
На фоне строгого соблюдения диеты приступы стали реже, тяжесть приступов уменьшилась.
Обсуждение
Гликогеноз IX типа является одним из редких заболеваний обмена веществ. Частота встречаемости 1:100 000 населения.
Гликогеноз IX типа (болезнь Хага) — наследственное заболевание, которое обусловлено дефицитом фермента киназы фосфорилазы, участвующего в обмене гликогена. Фосфокиназа состоит из 4 разных субъединиц, каждую из которых кодируют различные гены, располагающиеся в различных хромосомах и по-разному экспрессирующиеся в различных тканях: α (PHKA2), β (PHKAB), γ (PHKG2), δ (РНКА1). Субъединицы α и β выполняют регуляторные функции, γ — каталитическую функцию, а δ — функцию связывания ионов Са 2+ . Субъединица α имеет две изоформы — мышечную и печеночную, кодируемые двумя разными генами, располагающимися на Х-хромосоме. Гены, кодирующие остальные субъединицы, находятся в аутосомных хромосомах. Мутации в генах PHKA2, PHKAB и PHKG2 вызывают гликогеновую болезнь IXa, IXb и IXc типов соответственно. Тип IXa (с 2 подтипами — IXa1, IXa2) имеет Х-сцепленный вариант наследования, тогда как остальные — аутосомно-рецессивный.
Самыми частыми клиническими проявлениями являются гепатомегалия, задержка роста и моторного развития, гипотония, повышение активности трансаминаз. Вариабельность клинических проявлений зависит от характера мутации гена. В частности, при обследовании 6 детей с подтвержденным гликогенозом IX типа были выявлены разные мутации РНКА2 у каждого из них. Гепатомегалию имели все 6 детей, бессимптомные гипогликемические состояния — 2 из 6, задержка роста отмечалась у двоих, гиперлипидемия встречалась у 50% больных. Течение заболевания было относительно удовлетворительным [2]. Основными принципами лечения гликогеноза IX типа является специфическая гликогеновая диета, исключающая пищевой сахар, включающая белоксодержащие продукты (2,5 г белка на 1 кг массы тела в сутки), кукурузный крахмал в суточной дозе 1,5—3 г/кг в 3 приема [3, 4]. На фоне лечения у пациентов, как правило, отмечается положительная динамика в виде улучшения общего самочувствия, нормализации мышечного тонуса, нормализации размеров печени, показателей печеночных трансаминаз, купирования гипогликемий. Течение заболевания у большинства пациентов благоприятное, однако имеются случаи тяжелого течения с проявлениями кетоза, цирроза, тяжелых гипогликемий и печеночной недостаточности.
Заключение
Течение заболевания в описанном случае можно расценить как тяжелое, лабильное с частыми гипогликемическими состояниями, порой сопровождающееся потерей сознания, судорогами. Особенностями течения заболевания у данного пациента являются развитие тяжелых гипогликемических состояний, кетоза, высокие темпы роста, позднее развитие гепатомегалии, нормальный уровень трансаминаз. Вариабельность клинических проявлений коррелирует с различным характером мутаций у пациентов, возможной различной степенью пенетрантности поражаемых генов, вероятным сочетанием с другими мутациями.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Согласие пациента. Законный представитель ребенка (мать) дала добровольное согласие на публикацию клинического случая своего ребенка в журнал «Проблемы эндокринологии» в письменном виде
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Патогенез гликогенозов
Нарушения, вызванные мутациями структурных или регуляторных генов, ответственных за синтез и активность различных ферментов обмена гликогена, приводят к аномальному его накоплению и/или изменению его структуры – гликогенозу.
Ранее считалось, что из XI типов гликогенозов сердце поражается только при одном из них – II типе (сердечный гликогеноз). Теперь установлено, что сердце часто поражается и при III типе, а также в той или иной мере при IV, V и VI типах гликогенозов. С другой стороны, гликогенозы I,III,VI и VIII типов сопровождаются гипертриглицеридемией или смешанной гиперлипидемией, что предрасполагает к раннему развитию атеросклероза коронарных артерий [Schmitz G. с соавт.,1993].
Болезнь Помпе (гликогеноз II типа) наследственный дефицит кислой альфа-1,4-глюкозидазы (кислой мальтозы). Болезнь впервые описана Pompe в 1932 году. Кислая мальтоза локализуется в лизосомах и осуществляет гидролиз гликогена и других олигосахаридов до свободной глюкозы. Гликоген накапливается в лизосомах и цитоплазме миокарда (сократительном и в проводящей системе), скелетных мышц и печени. В сердце замещение миофибрилл гликогеновыми отложениями ведет к значительному увеличению его массы и размеров и к снижению его сократимости. Стенки желудочков и межжелудочковая перегородка концентрически утолщаются. В поздних стадиях возможна дилатация сердца.
Выделяют две формы заболевания: гликогеновую кардиомегалию грудных детей (гликогеноз IIa типа) и псевдомиотоническую форму (гликогеноз IIb). Гликогеноз IIa типа встречается значительно чаще, чем IIb тип. Возможно сочетание этих форм. Болезнью Помпе называют лишь первую – кардиальную форму.
В зависимости от времени появления симптоматики заболевания выделяют инфантильную, юношескую и взрослую формы. Заболевание преобладает у лиц мужского пола [Gullotta F., 1985] Ведущими экстракардиальными проявлениями при инфантильной форме являются генерализованная мышечная гипотония, снижение глубоких сухожильных рефлексов, затруднение дыхания, гепатомегалия, макроглоссия. У подростков и взрослых болезнь обычно проявляется прогрессирующей слабостью мышц тазового пояса, спинально отдела и диафрагмы.
Сердечно-сосудистая система. Заболевание развивается еще во внутриутробном периоде, при этом может быть внутриутробная смерть плода из-за тяжелой сердечной недостаточности приводящей к водянке плода [Atkin J., с соавт., 1984]. При инфантильной форме болезнь манифестирует в возрасте 2–7 мес. кардиомегалией с явлениями застойной сердечной недостаточности (выраженная гепатомегалия, цианоз конечностей, отеки) [Hwang B., с соавт.,1986].
В редких случаях начало болезни у новорожденных может проявиться патологической брадикардией [Van-Maldergem L., с соавт.,1990]. При аускультации обычно регистрируются тахикардия, ритм галопа, грубый систолический шум обструкции выходного тракта левого желудочка [Alday L.E., с соавт.,1984]. Однако в ряде случаев, несмотря на выраженную гипертрофию сердца контрактильная способность левого желудочка может длительное время находится в нормальных пределах. С другой стороны, описан вариант тяжелого течения гликогеноза у новорожденного без кардиомегалии [Ullrich K., с соавт.,1986].
При юношеской форме кардиомегалия может явиться случайной находкой при обследовании по поводу мышечной слабости, а хроническая сердечная недостаточность длительное время носит латентный характер.
При гликогенозе II типа может развиваться симптоматика легочной гипертензии с правожелудочковой недостаточностью. Последняя более характерна для взрослого типа IIb гликогеноза [Wiegand V., с соавт., 1986]. Она усиливается в ночные часы и связана с гиповентиляцией из-за прогрессирующего нервномышечного поражения диафрагмы [Budde-Steffen C., с соавт.,1989]. Наряду с этим, сердечная недостаточность прогрессирует из-за частых аспирационных пневмоний. Другим возможным проявлением гликогеноза II типа у подростков и взрослых является вакуольная дегенерация артериальных сосудов, иногда приводящая к субарахноидальному кровоизлиянию [Miyamoto Y., с соавт., 1985]. На ЭКГ характерна левожелудочковая или бивентрикулярная гипертрофия миокарда, высокий вольтаж комплексов QRS и зубцов Т, укороченный интервал P–R. Интервал Р–R в большинстве случаев укорочен до О,04–0,08 с, последний (синдром укороченного интервала P-R) предрасполагает к суправентрикулярной тахикардии [Fung K.P.,с соавт.,1989]. У 1/3 больных наблюдается отклонение электрической оси сердца влево, гипертрофия правого предсердия и правого желудочка. По данным О.М.Елисеева [1992] амплитуда RII+RIII (RI+SIII при отклонении оси сердца влево) высокая (превышает 30 мм, достигает 50-70 и даже 90 мм). Реже регистрируются узкие и глубокие зубцы Q в отведениях II, III, aVF, V4-V6. Могут обнаруживаться признаки нарушения внутрижелудочковой проводимости. Почти всегда имеются нарушения реполяризации в виде депрессии, реже подъема сегмента ST и симметричной инверсии зубца T, преимущественно в I, II и левых грудных отведениях. При юношеском типе и у взрослых может наблюдаться синдром WPW и атриовентрикулярная блокада I–II степени.
Рентгенологически определяется шаровидной формы тень сердца, кардиомегалия, преимущественно за счет левых отделов, усиление сосудистого рисунка легких.
При эхокардиографическом исследовании у новорожденных с гликогенозом IIa типа обнаруживается гипертрофия задней стенки левого желудочка и межжелудочковой перегородки, при этом полость левого желудочка, как правило, уменьшена. Данная гипертрофия может носить концентрический симметричный характер, или асимметричный при преимущественной гипертрофии межжелудочковой перегородки. При наличии асимметричной септальной гипертрофии появляется переднесистолическое движение митрального клапана, а при допплерографии регистрируется градиент давления между аортой и левым желудочком. Обычно, наряду с гипертрофией левого желудочка, определяется гипертрофия свободной стенки правого желудочка и увеличение его контрактильности [De-Dominicis E., с соавт.,1991; Shapir Y., с соавт., 1985].
По данным магниторезонансной томографии сердца определяются участки негомогенной плотности миокарда [Boxerm R.A., с соавт.,1986].
При аутопсии определяется значительное увеличение массы сердца из-за его гипертрофии. Сердечные камеры, коронарные артерии и клапаны не изменены. Может определяться умеренный эластофиброз эндокарда. При световой микроскопии определяется диффузная вакуолизация миокарда, в том числе в области проводящей системы сердца с накоплением в вакуолях гликогена. Электронная микроскопия выявляет аккумуляцию гликогена в пределах мембранозных структур и в саркоплазме.
Лабораторная диагностика: увеличение в крови креатининкиназы и лактатдегидрогеназы. Достоверные диагностические данные дает биопсия скелетной мышцы при гистологическом (вакуолизация), биохимическом (повышенное в несколько раз против нормы – 1,0-1,5 г/% – содержание гликогена), ферментном (отсутствие или чрезвычайно низкое содержание кислой мальтазы) и ультраструктурном исследовании (перегрузка гликогеном лизосом и цитоплазмы). Сниженное содержание кислой мальтазы определяют, кроме того, в биоптатах печени и в лейкоцитах, а также в фибробластах из культуры клеток кожи [О.М. Елисеев, 1992]. У большинства больных болезнью Помпе увеличена экспрессия предсердного натрий уретического пептида пропорционально величине гипертрофии миокарда [Benvenuti L.A., с соавт., 1994]. Лечение. При болезни Помпе летальный исход может быть несколько отсрочен введением кислой мальтазы, извлекаемой из плаценты человека или из культуры Aspergillus niger. Введением последнего экстракта удавалось временно нормализовать содержание гликогена в мышцах и длительность интервала Р–R на ЭКГ. Но, к сожалению, экзогенная кислая мальтаза, очевидно, не проникает в лизосомы и не может поэтому приостановить развитие болезни. Назначение дигоксина оказывается неэффективным, последний провоцирует желудочковые аритмии и развитие гипертрофии миокарда. При обструктивной форме кардиомиопатии оправдано в качестве симптоматической терапии длительное лечение бета- адреноблокаторами.
Тип наследования – аутосомно–рецессивный. Прогноз неблагоприятный, смерть при инфантильной форме наступает к концу второго года жизни, при ювенильной форме – до пубертатного периода.
Пренатальная диагностика осуществляется в культуре фибробластов, полученных при амниоцентезе. Гликогеноз III типа (Болезнь Кори, или болезнь Фербеса, лимитдекстриноз), возникает при врожденной недостаточности амило–1,6-глюкозидазы, в нормальных условиях содержащейся в большинстве тканей, в результате чего гликоген имеет аномальную структуру. Выделяют 2 типа болезни: гликогеноз IIIA типа – поражение печени и мышечной системы, IIIB – изолированное поражение печени (составляет примерно 15% среди всех больных с гликогенозом III типа).
Клиническая симптоматика заболевания появляется в возрасте 7-16 мес. Первоначально болезнь проявляется гепатомегалией, гипогликемией и задержкой развития, поэтому клинически не отличается от гликогеноза I типа. Затем симптоматика поражения печени исчезает и начинают доминировать миопатические признаки (мышечная гипотония, слабость дистальной мускулатуры, мышечные атрофии). Характерны также повторные респираторные инфекции, наклонность к ожирению. Могут определяться ксантомы на локтях, коленях, ягодицах, гиперлипидемия, увеличение уровня печеночных трансаминаз в крови, гипогликемические кризы. Течение может быть сравнительно благоприятным (больные живут 20 лет и более, если нет выраженного поражения сердца). Возможны непродолжительные ремиссии с уменьшением миопатической симптоматики и урежением частоты гипогликемических кризов.
Сердечно-сосудистая система. Поражение сердца наблюдается более, чем у 60% c гликогенозом IIIA и в детском возрасте протекает субклинически [Coleman R.A., с соавт.,1992]. У большинства выявляются электрокардиографические и эхокардиографические признаки гипертрофии левого желудочка при нормальных или несколько увеличенных рентгенографических границах сердца [Olson L.J., с соавт., 1984]. Гипертрофическая кардиопатия обычно носит необструктивный характер, реже наблюдаются обструктивные формы. Сердечная декомпенсация по застойному типу манифестирует с 13–15 летнего возраста [Moses S.W., с соавт.,1989]. Описаны случаи заболевания, проявляющиеся только тяжелой сердечной недостаточностью вследствие кардиомиопатии, без клинических проявлений миопатического процесса и поражения печени [Servidei S., с соавт.,1987].
На ЭКГ выявляются признаки гипертрофии левого желудочка, нарушение процесса реполяризации, реже – глубокий зубец Q, незначительное укорочение интервала Р-R. Рентгенологически выявляется умеренное увеличение тени сердца, так как гипертрофия левого желудочка носит преимущественно концентрический характер.
При эхокардиографическом исследовании определяется симметричная форма гипертрофической кардиомиопатии, нормальные или увеличенные размеры полости левого желудочка [Labrune P., с соавт.,1991]. Обструктивная форма гипертрофической кардиомиопати обычно не сопровождается высоким градиентом давления между аортой и левым желудочком [Carvalho J.S. с соавт.,1993].
Лабораторная диагностика. У большинства больных определяется гипогликемия, гиперлипидемия, увеличение уровня печеночных трансаминаз, креатининкиназы (свидетельствует о вовлечении в патологический процесс мышечной системы). В биоптатах мышц и печени обнаруживается перегрузка клеток гликогеном, снижение уровня амило-1,6-глюкозидазы при нормальном содержании кислой мальтазы [Е.Л. Розенфельд., с соавт. 1979]. В ряде случаев выявляется вторичное снижение активности таких ферментов, как глюкозо-6- фосфатаза или фосфорилаза. Лечение. Больным назначается диета, основанная на данных биохимического определения в крови содержания глюкозы, лактата и жиров. Поскольку глюконеогенез при этом заболевании не нарушен, обычно рекомендуется диета богатая белками. При развитии обструктивной формы гипертрофической кардиопатии назначается обзидан, симптоматическое лечение сердечной недостаточности (мочегонные, препараты калия, осторожно дигоксин).
Тип наследования: аутосомно – рецессивный.
Гликогеноз lV типа (Болезнь Андерсена , амилопектиноз) обусловлена дефицитом амило I,4,I,6-трансглюкозидазы. Аномальный гликоген накапливается в печени, почках, мышцах, селезенке, миокарде. Клиническая симптоматика. Заболевание возникает в периоде новорожденности и реже в раннем детстве. Основными экстракардиальными проявлениями являются гепатомегалия, с последующем развитием цирроза печени, спленомегалии, портальной гипертензии, варрикозного расширения вен пищевода, асцита. Обычно имеет место задержка соматического развития. В классических случаях болезнь быстро прогрессирует, смерть наступает в возрасте до 5 лет. Иногда может отмечаться гипогликемия, мышечная гипотония, мышечные атрофии. Сердечно сосудистая система. Поражение сердца наблюдается у половины больных и характеризуется дилатационной кардиомиопатией с выраженными проявлениями застойной сердечной недостаточности. В основном больные погибают в возрасте 1–2 лет, однако известны случаи дилатационной кардиомиопатии, при которых больные жили до12 лет [De-La- Blanchardiere A. с соавт.,1994]. При аутопсии определяется типичная картина дилатационной кардиомиопатии, выраженный фиброз и базофильная дегенерация кардиомиоцитов, умеренная их гипертрофия, внутриклеточные включения телец, содержащих аномальный гликоген [Tamura S., с соавт.,1995 ].
При эхокардиографическом исследовании определяется картина дилатационной кардиомиопатии, левый и правый желудочек значительно дилатированы, резко снижена их контрактильная функция. Имеются единичные описания так называемого ювенильного амилопектиноза с сердечно-мышечной миопатией. Поражение сердца проявляется симметричной гипертрофической кардиомиопатией. Продолжительность жизни таких детей достигает 13–15 лет [Tunon T., с соавт., 1988; Greene G.M., с соавт., 1987]. Лечение гликогеноза IV типа не разработано. Коррекция сердечной недостаточности сердечными гликозидами и диуретиками оказывает временный эффект.
Пренатальная диагностика проводится по результатам обследования на аномальный гликоген в культивированных клетках амниотической жидкости и позволяет предупреждать рождение обреченных на раннюю смерть детей.
Тип наследования: аутосомно–рецессивный.
Гликогеноз V типа (Болезнь Мак-Ардля) развивается из-за недостатка мышечной фосфорилазной активности, в связи с чем гликоген накапливается в избытке в мышцах.
Клиническая симптоматика. Слабовыраженные признаки болезни в виде сниженной двигательной активности, плохой переносимости физических нагрузок появляется в 6-10 лет. Затем, обычно в подростковом возрасте, появляются слабость, боли в мышцах, мышечная ригидность при нагрузках, часто выявляется миоглобинурия. Характерен феномен “второго окна”, когда мышечные боли, провоцирующиеся физической нагрузкой исчезают через несколько минут, даже если нагрузка не прекращена. Этот феномен объясняется активацией метаболизма свободных жирных кислот.
Сердечно-сосудистая система. Поражение сердечно- сосудистой системы обычно протекает латентно в виде функциональных нарушений.
На ЭКГ может обнаруживаться: синусовая брадикардия, удлинение интервала Р–R, увеличение амплитуды комплекса QRS. Лабораторная диагностика: При проведении физической нагрузки в плазме крови обнаруживается увеличение активности креатининкиназы и трансаминаз. Наряду с этим, из-за усиления деградации мышечных пуриновых нуклеотидов в крови возрастает содержание инозина, гипоксантина, мочевых кислот, аммиака. Окончательный диагноз устанавливается при мышечной биопсии с определением ферментной активности.
Прогноз при болезни Мак-Ардля благоприятный, однако необходима соответствующая профессиональная ориентация больных.
Лечение: рекомендуется назначение диеты с высоким содержанием протеинов. Показано курсовое лечение препаратами АТФ, цитохрома С.
Тип наследования: аутосомно–рецессивный.
Гликогеноз VI типа (болезнь Херса) возникает при дефиците печеночной фосфорилазы. В печени образуется достаточное количество гликогена с нормальной структурой, но он не может метаболизироваться из-за энзимного дефекта. Клиническая симптоматика. Заболевание проявляется замедлением роста, гепатомегалией, повышением активности аминотрансфераз, содержания холестерина, а также триглицеридов в сыворотке крови. Возможны нерезко выраженные гипогликемические состояния.
Сердечно-сосудистая система. Поражение сердечно– сосудистой системы обычно протекает латентно в виде функциональных нарушений. Могут обнаруживаться изменения ЭКГ (нарушение процесса реполяризации, увеличение вольтажа комплекса QRS, укорочение интервала P–R при отсутствии клинических признаков поражения сердца.
Прогноз при гликогенозе VI типа благоприятный. По- видимому, нарушения в обмене гликогена, вызванные дефектом печеночной фосфорилазы, могут компенсироваться за счет глюконеогенеза.
Тип наследования: аутосомно – рецессивный.
Дефицит сердечной фосфорилазкиназы (изолированный гликогеноз сердца)
Клиническая симптоматика характеризуется ранним развитием кардиомегалии и сердечной недостаточности [Eishi Y., с соавт.,1985]. На ЭКГ регистрируется укорочение интервала P–R, увеличение вольтажа QRS комплекса, депрессия сегмента S–T с инверсией зубца Т, глубокий зубец Q. Эхокардиография выявляет увеличение толщины миокарда задней стенки левого желудочка, межжелудочковой перегородки и правого желудочка, дилатацию предсердий. При аутопсии в сердечной мышце определяется большое отложение структурно нормального гликогена, при этом депозиты гликогена отсутствуют в скелетной мышце и печени (изолированный гликогеноз сердца). Электронная микроскопия выявляет разрывы миофибрилл, депозитыгранул гликогена в цитоплазме.
Лабораторная диагностика. При ферментном анализе активность мальтазы, амило-1,6-глюкозидазы и фосфорилазы в сердце, скелетной мышце и печени не нарушена. В сердечной мышце полностью отсутствует активность фосфорилазкиназы, в то время как в скелетной мышце и печени она нормальная.
Прогноз неблагоприятный, больные погибают в возрасте 5 мес.- 3 лет от прогрессирующей сердечной недостаточности [Elleder M. С соавт.,1993].
Лечение не разработано.
Тип наследования: аутосомно–рецессивный.
Лизосомальный гликогеноз с сердечно-мышечной миопатией. Клиническая симптоматика. Болезнь развивается в раннем возрасте и проявляется задержкой умственного развития, умеренной миопатией и кардиомиопатией [Byrne E., с соавт., 1986]. У мальчиков более выражена миопатия, у девочек происходит преимущественное поражение сердца при минимальных системных проявлений болезни [Dworzak F. с соавт., 1994].
Сердечно-сосудистая система. Во всех сообщенных случаях определялась симметричная гипертрофическая кардиомиопатия с выраженными проявлениями застойной сердечной недостаточности. При биопсии скелетной и сердечной мышцы обнаруживается вакуольная миопатия со значительным отложением свободного и внутрилизосомального гликогена. При морфологическом исследовании сердца определяется кардиомиопатия с дилатацией и гипертрофией преимущественно левого желудочка, распространенный миокардиальный фиброз.
Лабораторная диагностика: Характер ферментного дефекта до настоящего времени не установлен. При ферментологическом исследовании активность кислой мальтазы и фосфорилазы в пределах нормы [Bru Р., с соавт., 1988].
Лечение не разработано. Сиптоматическое лечение застойной сердечной недостаточности оказывает временное улучшение. Сообщены случаи успешной пересадки сердца у таких больных [Dworzak F. С соавт., 1994].